题目内容
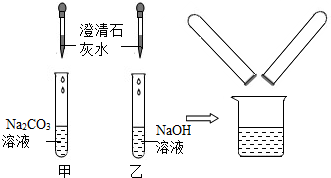
老师为了辨别一瓶失去标签的溶液时碳酸钠还是氢氧化钠进行了如图所示的两个实验,实验结束后,老师将试管中的废液倒入同一个干净的烧杯中茗茗看到废液变浑浊,就对废液进行了过滤,并和几位同学对滤液的成分又进行了探究.
【提出问题】滤液中只含NaOH:
【猜想与假设】
甲同学认为:滤液中只含NaOH
乙同学认为:滤液中可能含有NaOH和Na2CO3
丙同学认为:滤液中可能含有NaOH,Na2CO3和Ca(OH)2
【讨论】
(1)图甲中,发生反应的化学方程式为______;
(2)你认为上述猜想不合理的是______,理由是______;
【实验分析】经过与同学的商量后,茗茗决定针对乙同学的猜想进行实验,实验过程如下表所示,请将表格补充完整
【提出问题】滤液中只含NaOH:
【猜想与假设】
甲同学认为:滤液中只含NaOH
乙同学认为:滤液中可能含有NaOH和Na2CO3
丙同学认为:滤液中可能含有NaOH,Na2CO3和Ca(OH)2
【讨论】
(1)图甲中,发生反应的化学方程式为______;
(2)你认为上述猜想不合理的是______,理由是______;
【实验分析】经过与同学的商量后,茗茗决定针对乙同学的猜想进行实验,实验过程如下表所示,请将表格补充完整
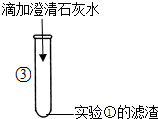
| 实验操作 | 取适量滤液于试管中,向其中加入酸性溶液①______ |
| 实验现象 | ②______ |
| 实验结论 | 乙同学的猜想成立 |

(1)碳酸钠和氢氧化钙反应生成白色的碳酸钙沉淀和氢氧化钠,反应的方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(2)碳酸根离子和钙离子会直接反应生成碳酸钙沉淀.所以,丙猜想不合理,因为Na2CO3和Ca(OH)2能发生反应,不能共存;
实验分析:若猜想乙成立,则滤液中含有NaOH和Na2CO3,验证时可加稀盐酸,并且一开始不冒出气泡,因为盐酸消耗掉滤液中的NaOH才能和Na2CO3反应冒出气泡.
故答为:(1)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(2)丙猜想不合理,因为Na2CO3和Ca(OH)2能发生反应,不能共存;实验分析:①稀盐酸;②一段时间后,有气泡冒出.
(2)碳酸根离子和钙离子会直接反应生成碳酸钙沉淀.所以,丙猜想不合理,因为Na2CO3和Ca(OH)2能发生反应,不能共存;
实验分析:若猜想乙成立,则滤液中含有NaOH和Na2CO3,验证时可加稀盐酸,并且一开始不冒出气泡,因为盐酸消耗掉滤液中的NaOH才能和Na2CO3反应冒出气泡.
故答为:(1)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(2)丙猜想不合理,因为Na2CO3和Ca(OH)2能发生反应,不能共存;实验分析:①稀盐酸;②一段时间后,有气泡冒出.

练习册系列答案
相关题目