题目内容
【题目】海洋是巨大的资源宝库,人类提取海水中的化学元素,来制备有多种用途的物质.广泛应用于火箭、导弹和飞机制造业的金属镁,就是利用从海水中提取的镁盐制取的.工业上从海水中提取单质镁的过程如图所示:
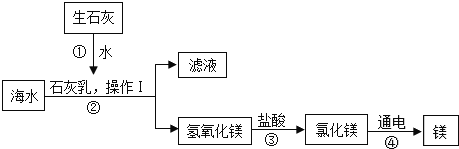
(1)在上述转化过程中发生分解反应的化学方程式是_____.
(2)海水中本身就含有氯化镁,请分析①、②两步的目的是_____.
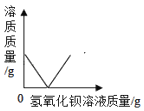
(3)小明同学在实验室中用NaOH溶液替代石灰乳模拟生产过程中的第①步.他取NaCl和MgCl2的固体混合物25克,加入适量水完全溶解后,与溶质质量分数为20%的NaOH溶液混合充分反应,记录的生成的沉淀与加入的NaOH溶液质量关系如图所示:
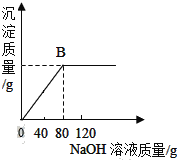
①当滴入上述NaOH溶液至图中B点时,烧杯中溶液里含有的溶质为_____(写化学式).
②原混合物中MgCl2的质量为_____g.
③当滴入上述NaOH溶液100g时,试通过计算,求此时烧杯中所得不饱和溶液中NaCl溶质质量分数_____(计算结果精确至0.1%)。
【答案】MgCl2 Mg+Cl2↑ 富集MgCl2,得出纯净的MgCl2 NaCl 19 25.9%
Mg+Cl2↑ 富集MgCl2,得出纯净的MgCl2 NaCl 19 25.9%
【解析】
氯化镁通电生成镁和氯气,氢氧化钠和氯化镁反应生成氢氧化镁和氯化钠。
(1)在上述转化过程中发生分解反应是氯化镁通电生成镁和氯气,反应的化学方程式是MgCl2![]() Mg+Cl2↑。
Mg+Cl2↑。
(2)海水中含有氯化镁,氯化镁溶解在海水中,不能直接提取出来,经过①、②两步将海水中的镁离子提取出来,得到纯净的氯化镁,然后电解得到氯化镁,故①、②两步的目的是富集MgCl2,得出纯净的MgCl2。
(3)①氢氧化钠和氯化镁生成氢氧化镁沉淀和氯化钠,当滴入上述NaOH溶液至图中B点时,烧杯中溶液里含有的溶质为氯化钠,化学式为NaCl。
②设原混合物中MgCl2的质量为x

![]()
![]()
故原混合物中MgCl2的质量为19g。
③设生成的氯化钠的质量为y,生成氢氧化镁的质量为z
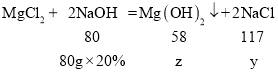
![]()
![]()
当滴入上述NaOH溶液100g时,烧杯中所得不饱和溶液中NaCl溶质质量分数为
![]()

 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案