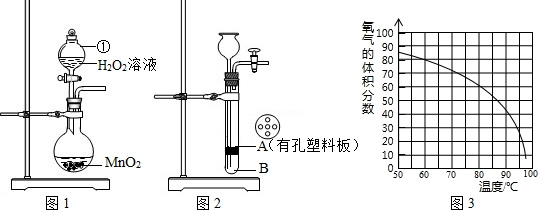
题目内容
如表是某研究性学习小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
请分析回答:
(1)该研究小组在设计实验方案时,考虑了①
(2)从上述影响过氧化氢分解速率的因素中任意选择一种说明该因素对其分解速率有何影响?
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总重量
| 溶度 时间(S) 反应条件 |
30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360 | 480 | 540 | 720 |
| MnO2催化、不加热 | 10 | 25 | 60 | 120 |
(1)该研究小组在设计实验方案时,考虑了①
温度
温度
、②催化剂
催化剂
、③反应物的浓度
反应物的浓度
等因素对过氧化氢分解速率的影响.(2)从上述影响过氧化氢分解速率的因素中任意选择一种说明该因素对其分解速率有何影响?
温度越高,过氧化氢的分解速率越快(或过氧化氢浓度越高,过氧化氢的分解速率越快或使用催化剂,过氧化氢的分解速率越快)
温度越高,过氧化氢的分解速率越快(或过氧化氢浓度越高,过氧化氢的分解速率越快或使用催化剂,过氧化氢的分解速率越快)
.(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总重量
不变
不变
(选填“减小”或“不变”或“增大”).分析:本题对影响过氧化氢(H2O2)分解速率的因素进行探究,首先用不同溶质质量分数的H2O2溶液,在无催化剂不加热条件下分解情况时;其次无催化剂加热条件下的分解情况;再次是加入MnO2并且加热条件下的分解情况,根据实验数据很容易找到规律.
解答:解:(1)根据表中给出的数据,无催化剂不加热的情况下,不同浓度的过氧化氢溶液都是几乎不反应,在无催化剂加热的情况下,不同浓度的过氧化氢溶液都分解,说明过氧化氢的分解速率与温度有关,但是得到相同气体的时间不同,浓度越大,反应的速度越快,说明过氧化氢的分解速率与浓度有关;比较同一浓度的过氧化氢溶液如30%时,在无催化剂加热的时候,需要时间是360s,有催化剂加热的条件下,需要时间是10s,说明过氧化氢的分解速率与温度、催化剂、反应物的浓度因素有关;故答案为:温度;催化剂;反应物的浓度;
(2)在无催化剂不加热条件下不分解,而在无催化剂加热条件下的分解,说明温度对过氧化氢分解速率的影响;
故答案为:温度越高,过氧化氢的分解速率越快(或过氧化氢浓度越高,过氧化氢的分解速率越快或使用催化剂,过氧化氢的分解速率越快);
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总重量不变.故填:不变.
(2)在无催化剂不加热条件下不分解,而在无催化剂加热条件下的分解,说明温度对过氧化氢分解速率的影响;
故答案为:温度越高,过氧化氢的分解速率越快(或过氧化氢浓度越高,过氧化氢的分解速率越快或使用催化剂,过氧化氢的分解速率越快);
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总重量不变.故填:不变.
点评:本题通过对比实验结果的分析,找到事物的内在联系,是考查学生的分析问题的能力,同时也是对“影响反应速率因素”这一知识点进行了较深入的分析.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
 利用纯碱在实验室可以制取许多物质,某研究性学习小组对纯碱展开如下探究:
利用纯碱在实验室可以制取许多物质,某研究性学习小组对纯碱展开如下探究:
Ⅰ.利用纯碱和稀盐酸制取二氧化碳
(1)写出如图装置B中标号仪器名称______,用纯碱和稀盐酸制取二氧化碳的反应方程式为______.应该选用的发生装置为______,用装置C收集二氧化
碳导气管需伸到集气瓶底部,目的______.
(2)有人认为用稀硫酸和纯碱制取二氧化碳,优于用稀盐酸和纯碱制取二氧化碳,理由是______.
Ⅱ.利用纯碱和熟石灰制取烧碱溶液
步骤一:将纯碱溶于水,加入适量熟石灰;步骤二:过滤;步骤三:检验滤液中存在的溶质.
(3)步骤一中需要使用玻璃棒,其作用是______,纯碱与熟石灰反应方程式为______.
(4)步骤二中过滤器中滤纸没有紧贴漏斗内壁的后果是______.
(5)小红按下表完成步骤三,请你将小红的实验设计补充完整
| 实验操作 | 实验现象 | 实验结论 | |
| ① | 取少量滤液,滴入纯碱溶液 | 没有白色沉淀产生 | |
| ② | 另取少量滤液,滴入,静置. | 含有碳酸钠 和氢氧化钠 |
利用纯碱在实验室可以制取许多物质,某研究性学习小组对纯碱展开如下探究:
Ⅰ.利用纯碱和稀盐酸制取二氧化碳
(1)写出如图装置B中标号仪器名称______,用纯碱和稀盐酸制取二氧化碳的反应方程式为______.应该选用的发生装置为______,用装置C收集二氧化
碳导气管需伸到集气瓶底部,目的______.
(2)有人认为用稀硫酸和纯碱制取二氧化碳,优于用稀盐酸和纯碱制取二氧化碳,理由是______.
Ⅱ.利用纯碱和熟石灰制取烧碱溶液
步骤一:将纯碱溶于水,加入适量熟石灰;步骤二:过滤;步骤三:检验滤液中存在的溶质.
(3)步骤一中需要使用玻璃棒,其作用是______,纯碱与熟石灰反应方程式为______.
(4)步骤二中过滤器中滤纸没有紧贴漏斗内壁的后果是______.
(5)小红按下表完成步骤三,请你将小红的实验设计补充完整

Ⅰ.利用纯碱和稀盐酸制取二氧化碳
(1)写出如图装置B中标号仪器名称______,用纯碱和稀盐酸制取二氧化碳的反应方程式为______.应该选用的发生装置为______,用装置C收集二氧化
碳导气管需伸到集气瓶底部,目的______.
(2)有人认为用稀硫酸和纯碱制取二氧化碳,优于用稀盐酸和纯碱制取二氧化碳,理由是______.
Ⅱ.利用纯碱和熟石灰制取烧碱溶液
步骤一:将纯碱溶于水,加入适量熟石灰;步骤二:过滤;步骤三:检验滤液中存在的溶质.
(3)步骤一中需要使用玻璃棒,其作用是______,纯碱与熟石灰反应方程式为______.
(4)步骤二中过滤器中滤纸没有紧贴漏斗内壁的后果是______.
(5)小红按下表完成步骤三,请你将小红的实验设计补充完整
| 实验操作 | 实验现象 | 实验结论 | |
| ① | 取少量滤液,滴入纯碱溶液 | 没有白色沉淀产生 | ______ |
| ② | 另取少量滤液,滴入______,静置. | ______ | 含有碳酸钠 和氢氧化钠 |

 27、利用纯碱在实验室可以制取许多物质,某研究性学习小组对纯碱展开如下探究:
27、利用纯碱在实验室可以制取许多物质,某研究性学习小组对纯碱展开如下探究: