题目内容
【题目】为测定空气中氧气的含量,小华和小强同学分别设计如下方案:
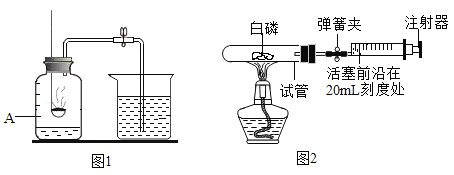
小华:采用图1装置进行实验.(燃烧匙中药品为红磷)
小强:图2将过量的白磷放入试管,通过导管与针筒注射器组成如图的实验装置.用小华设计实验,回答问题:
(1)红磷在集气瓶中燃烧的现象为_____化学式反应式为_____。
(2)待燃烧停止,装置冷却后,打开止水夹,观察到进入集气瓶中水的体积不到总容积的1/5,你认为其原因可能是_____(写2点)。
(3)如将燃烧匙中红磷换成硫粉,能否成功?为什么?_____。
(4)图2的设计操作与图1比较,其优点是_____(写2点)。
【答案】产生大量白烟,放出热量 4P+5O2![]() 2P2O5 红磷的量不足、装置漏气等 不能,硫燃烧产生二氧化硫气体,集气瓶内的压强不变 减少空气污染,结果更准确
2P2O5 红磷的量不足、装置漏气等 不能,硫燃烧产生二氧化硫气体,集气瓶内的压强不变 减少空气污染,结果更准确
【解析】
(1)磷与氧气在点燃的条件下反应生成五氧化二磷,燃烧的现象为产生大量白烟,放出热量;故填:产生大量白烟,放出热量;4P+5O2![]() 2P2O5;
2P2O5;
(2)集气瓶中的液面不能上升五分之一,可能的原因是气密性不良好、红磷不足量、反应不充分、未等到冷却至室温就在打开止水夹.故填:红磷的量不足;装置漏气等;
(3)硫燃烧生成二氧化硫气体,造成集气瓶内的压强不变,所以打开止水夹后烧杯中的水也不会进入集气瓶,无法测定空气中氧气的含量;故填:不能,硫燃烧产生二氧化硫气体,集气瓶内的压强不变;
(4)图2的设计操作与图1比较,它可以防止磷燃烧产生的白烟散逸到空气中,再就是装置的刻度更清楚,读数更容易;故填:减少空气污染,结果更准确;

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目