题目内容
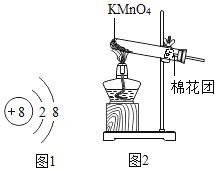
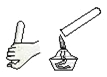
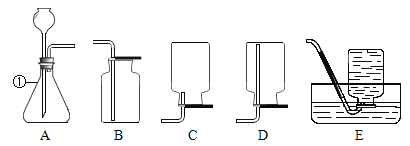
【题目】某校研究性学习小组用下图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%。
(1)图中A仪器的名称是________,燃烧、冷却后打开止水夹,水能进入集气瓶的原因是_____________。
(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的_____%。现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有氮气。
(发现问题)氮气是怎样减少的呢?
(假设一)氮气与镁条反应而减少。
(假设二)__________。
(查阅资料)镁条在氮气中能燃烧,产物为氮化镁(Mg3N2)固体。氮化镁中氮元素的化合价为_________。
镁条还可以在二氧化碳气体中燃烧生成碳和氧化镁,该反应化学方程式是__________。
(拓展延伸)由此你对燃烧的新认识________
【答案】烧杯 集气瓶内气体减少,导致压强减小,水沿导管进入瓶内 21% 氮气与铁丝反应而减少 -3 2Mg+CO2![]() 2MgO+C。 燃烧不一定有氧气参加反应
2MgO+C。 燃烧不一定有氧气参加反应
【解析】
(1)镁燃烧消耗瓶内气体生成固体物质,瓶内气体减少,压强减小。据此分析回答;
(2)氧气约占空气体积分数的21%,氮气占78%,如果镁燃烧只消耗氧气时,气体减少原体积的21%;
假设二:根据瓶内物质可能与氮气反应进行分析解答;
查阅资料:根据化合价规律和化学方程式的书写方法进行分析解答;
拓展延伸:根据实验现象进行分析解答。
(1)图中A仪器的名称是烧杯,镁条燃烧时会与空气中的氧气反应生成固体氧化镁,致使瓶内气体减少压强减小,水在大气压作用下进入瓶中;
(2)空气中氧气的体积分数为21% 。如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的21%。现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有氮气;
假设二:氮气的减少可能是镁与氮气反应而减少,也可能是氮气与铁丝反应而减少。所以假设二可以是: 氮气与铁丝反应而减少;
查阅资料:①设:氮元素的化合价为x,根据化合物中各元素化合价的代数和为零,则有:(+2)×3+2x=0,解得x=-3;
②根据题意,镁条还可以在二氧化碳气体中燃烧,生成碳和氧化镁,反应的方程式为:2Mg+CO2![]() 2MgO+C;
2MgO+C;
拓展延伸:由镁不仅能在氧气中燃烧,也能在二氧化碳、氮气中燃烧,可以得出燃烧不一定有氧气参加反应。

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案【题目】某兴趣小组同学对实验室制氧气的条件进行如下探究:
(a)为探究催化剂的种类对氯酸钾分解速率的影响,甲设计以下对比实验:
①将3.0g氯酸钾和1.0g二氧化锰均匀混合加热;
②将xg氯酸钾和1.0g氧化铜均匀混合加热。
在相同温度下,比较两组实验产生氧气的快慢。
①中反应的化学方程式是__________________________;②中x的值应为_____。
(猜想)除二氧化锰,氧化铜外,Fe2O3也可以做氯酸钾分解的催化剂。
按下表进行实验:测定分解温度(分解温度越低,催化效果越好)
实验编号 | 实验药品 | 分解温度/℃ |
① | 氯酸钾 | 580 |
② | 氯酸钾、二氧化锰(质量比1∶1) | 350 |
③ | 氯酸钾、氧化铜(质量比1∶1) | 370 |
④ | 氯酸钾、Fe2O3(质量比1∶1) | 390 |
由实验________与实验④对比,证明猜想合理。实验所用的三种金属氧化物,催化效果最好的是___。
(b)乙探究了影响过氧化氢溶液分解速率的某种因素。实验记录如下:
过氧化氢溶液的质量 | 过氧化氢的浓度 | 二氧化锰的质量 | 相同时间内产生VO2 | |
① | 50.0g | 1% | 0.1g | 9mL |
② | 50.0g | 2% | 0.1g | 16mL |
③ | 50.0g | 4% | 0.1g | 31mL |
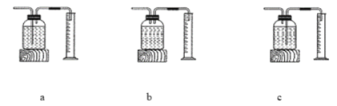
实验结论:在相同条件下,_______________________________,过氧化氢分解得越快。本实验中测量O2体积的装置(如图)应该选择:_______。(填字母)