题目内容
强化安全意识,提升安全素养。下列采取的安全措施错误的是( )
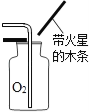
A. 不必检纯度,直接点燃一氧化碳
B. 在火灾逃生时用湿毛巾捂住口鼻,并匍匐前进
C. 在加油站张贴严禁烟火标志
D. 用天然气作燃料,在燃气灶的厨房内上方安装报警器
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案合成氨是人类科学技术上的一项重大突破,对社会发展与进步做出了巨大贡献。合成氨的工艺流程图如下:

(1)该工艺流程中能循环利用的物质是_____________。
(2)写出变化②中N2、H2反应生成NH3的符号表达式:_________________________。
(3)将沸点不同的气体分离开来,常采用液化分离法。如本流程中将产物NH3与N2、H2分离开来的最适宜的温度是-33.35℃。则根据下表判断,变化①将空气中N2与O2分离时最适宜的温度是________℃。变化①属于__________变化。
物质 | H2 | N2 | O2 | NH3 |
沸点/℃ | -252 | -195.8 | -183 | -33.35 |
为了测定某石灰石样品中碳酸钙的含量,取20g此样品,将80g的稀盐酸分四次加入样品使之充分反应(石灰石中的杂质不溶于水,也不与盐酸及生成物反应),每次用盐酸的质量与反应后剩余固体的质量见下表.(计算结果保留到小数点后一位数字)
次 数 | 一 | 二 | 三 | 四 |
加入盐酸的质量/g | 20 | 20 | 20 | 20 |
剩余固体的质量/g | 15 | 10 | 5 | 5 |
计算:(1)样品中碳酸钙的质量分数____;
(2)20g此样品与足量盐酸反应最多生成二氧化碳的质量____;
(3)加入的稀盐酸中溶质的质量分数____.
下列实验操作不能达到实验目的的是
选项 | 实验目的 | 实验操作 |
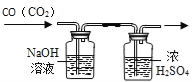
A | 除去氧气中少量的水蒸气 | 通过盛有浓硫酸的洗气瓶 |
B | 除去NaCl溶液中的Na2CO3 | 加适量稀硫酸 |
C | 鉴别①CuSO4溶液②FeCl3溶液③NaCl溶液 ④NaOH溶液 | 不加其它试剂,利用组内物质的颜色和相互反应进行鉴别 |
D | 除去稀盐酸中混有的少量硫酸 | 加入适量的BaCl2溶液,再过滤 |
A. A B. B C. C D. D
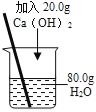
某学习小组在帮助实验员整理化学试剂时发现了一瓶标签残缺的无色溶液,(如图所示),经实验员分析可知原瓶溶液中的溶质可能是 NaHCO3,NaOH,Na2CO3,NaCl中的一种,请你对该试剂作出猜想并进行实验探究:
(提出问题)这瓶试剂是什么溶液?
(猜想与假设)
甲猜想:NaHCO3溶液
乙猜想:NaOH溶液
丙猜想:Na2CO3溶液
丁猜想:NaCl溶液
(查阅资料)上述四种物质相关信息如下
物质 | NaHCO3 | NaOH | Na2CO3 | NaCl |
常温下溶解度/g | 9.6 | 109 | 21.5 | 36 |
常温下稀溶液的pH | 9 | 13 | 11 | 7 |
(实验探究1)取瓶中溶液少许于试管中,滴加几滴酚酞溶液,溶液变红。
(实验探究2)另取瓶中溶液少许于试管中,滴加足量的稀盐酸,产生生气泡。
(实验分析)通过(实验探究1)可知_____同学的猜想一定错误。
甲同学仔细分析四种物质的相关信息表后发现自已的猜想错误,他的理由是_____。
丙同学分析(实验探究2)并结合以上同学的实验结论,认为原瓶溶液是NaCO3溶液。
(实验探究2)中发生反应的化学方程式为_____。
(讨论质疑)乙认为以上同学分析有漏洞,需要进一步实验确定,于是又进行了如下探究。
(实验探究3)在(实验探究1)试管中的红色溶液中滴加过量氯化钙溶液(中性),充分反应后,试管中溶液仍呈红色,但有白色沉淀产生。
(得出结论)通过(实验探究3)可证明这瓶试剂为_____溶液,但已经部分变质。
(反思与拓展)学习小组反思了这瓶试剂因为_____而变质,得出了该溶液正确的保存方法,若要除去该溶液变质部分所采用的方法是_____(用化学反应方程式表示)。

在探究氢氧化钙与稀盐酸中和反应实验时,忘记了滴加酚酞溶液,无法判断反应进行到何种程度,同学们决定对反应后溶液中溶质的成分进行探究。
请写出该反应的化学方程式。_____
(提出问题)反应后溶液中的溶质是什么?
(做出猜想)猜想一:CaCl2 和 Ca(OH)2 猜想二:CaCl2 和 HCl猜想三:_____
(设计方案)
实验操作 | 实验现象 | 实验结论 |
①取少量反应后的溶液于试管中,滴加酚酞试液 | _____。 | 猜想一不正确 |
②另取少量反应后的溶液于试管中,加入_____。 | _____。 | 猜想二不正确 |
(拓展与应用)将稀盐酸逐滴匀速加入一定量的稀氢氧化钙溶液中,用数字化仪器对反应过程中溶液的温度、pH 进行实时测定,得到的曲线如图 1、图2所示。

由图 1、图2知,稀盐酸与稀氢氧化钙溶液已发生中和反应的判断依据是_____。