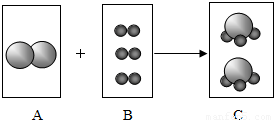题目内容
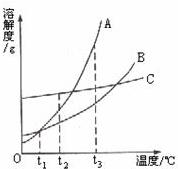 (2007?沈阳)如图中是A、B、C三种固体物质的溶解度曲线.请根据图象回答下列问题:
(2007?沈阳)如图中是A、B、C三种固体物质的溶解度曲线.请根据图象回答下列问题:(1)在A、B、C三种物质中,溶解度受温度影响变化不大的物质是
C
C
;(2)在t2℃时,A、B、C三种物质的溶解度由大到小的顺序是
C>A>B
C>A>B
;(3)相同质量的A、B两种物质的饱和溶液,温度从t3℃降低至t1℃时,析出晶体质量较多的是
A
A
.分析:根据固体物质的溶解度曲线可以:①比较不同物质在同一温度下的溶解度的大小,②判断物质的溶解度随温度变化的变化情况,从而确定等质量的饱和溶液降温时析出晶体的多少.
解答:解:(1)由三种物质的溶解度曲线不难看出,C的溶解度受温度的影响最小,故答案为:C
(2)由三物质的溶解度曲线可知,在在t2℃时,三种物质的溶解度的大小关系是C>A>B,故答案为:C>A>B
(3)由于三种物质的溶解度都随温度的升高而增大,但是A的溶解度受温度的影响最大,因此相同质量的A、B两种物质的饱和溶液,温度从t3℃降低至t1℃时,A的溶液中析出的晶体最多,故答案为:A
(2)由三物质的溶解度曲线可知,在在t2℃时,三种物质的溶解度的大小关系是C>A>B,故答案为:C>A>B
(3)由于三种物质的溶解度都随温度的升高而增大,但是A的溶解度受温度的影响最大,因此相同质量的A、B两种物质的饱和溶液,温度从t3℃降低至t1℃时,A的溶液中析出的晶体最多,故答案为:A
点评:本题难度不是很大,主要考查了固体溶解度曲线的意义,加深学生对固体溶解度的理解,培养学生的分析能力和解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 表示氮原子,
表示氮原子, 表示氢原子.请你根据图示回答下列问题:
表示氢原子.请你根据图示回答下列问题: