题目内容
【题目】化学学科实践活动课上,老师拿来一包粉末。它是由长期放置在空气中的铁粉和久置的碱石灰干燥剂混合而成,让同学们设计实验进行探究。
(提出问题)固体样品的成分是什么?
(查阅资料)(1)碱石灰干燥剂是CaO和NaOH的混合物。
(2)BaCl2溶液显中性。
(猜想与假设)固体样品中可能含有 Fe、Fe2O3、CaO、NaOH、Ca(OH)2、Na2CO3和_____等七种物质。
(进行实验)
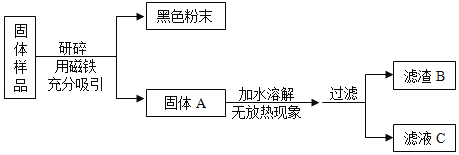
甲组同学对滤渣B的成分进行探究,记录如下:
实验操作 | 实验现象 | 实验结论及化学方程式 |
取少量滤渣B于试管中,加入足量稀盐酸,将生成的气体通入澄清的石灰水中 | ①_____ ②_____ | 结论:滤渣B中有 Fe2O3,CaCO3.实验操作中反应的化学方程式为:_____(答出一个即可) |
乙组同学对滤液C的成分进行探究,记录如下:
实验操作 | 实验现象 | 实验结论 |
取少量滤液C于试管中,加入过量BaCl2溶液,静置,向上层清液中滴加无色酚酞试液,振荡 | ①有白色沉淀生成 ②酚酞试液由无色变成红色 | 滤液C中有_____ |
(解释与结论)(1)乙组同学实验中加入过量BaCl2溶液的目的是_____。
(2)通过以上实验探究,该固体样品中能确定一定含有的成分是_____。
【答案】CaCO3固体全部溶解,溶液由无色变成黄色澄清石灰水变浑浊Fe2O3+6HCl═2FeCl3+3H2O(答出一个即可)NaOH、Na2CO3使碳酸钠完全反应,以防止对检验氢氧化钠产生影响Fe、Fe2O3、Ca(OH)2、Na2CO3
【解析】
铁能被磁铁吸引,生锈产生氧化铁,氧化铁和稀盐酸反应生成氯化铁和水,氧化钙和水反应生成氢氧化钙,氢氧化钙和二氧化碳反应生成碳酸钙和水,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钡反应生成白色沉淀碳酸钡和氯化钠;氢氧化钠溶液、氢氧化钙溶液、碳酸钠溶液都是显碱性溶液,都能使酚酞试液变红色。
猜想与假设:
氧化钙吸收空气中的水生成氢氧化钙,氢氧化钠吸收空气中的二氧化碳生成碳酸钠,碳酸钠能与氢氧化钙反应生成物碳酸钙和氢氧化钠。所以固体样品中可能含有 Fe、Fe2O3、CaO、NaOH、Ca(OH)2、Na2CO3和CaCO3等七种物质;
进行实验:
甲组:若固体中含有氧化铁,加入足量稀盐酸,稀盐酸和氧化铁反应生成氯化铁和水,氯化铁溶液呈黄色,实验现象是固体全部溶解,溶液由无色变成黄色;若固体中含有碳酸钙,加入足量稀盐酸,稀盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,二氧化碳能使澄清的石灰水变浑浊,实验现象是澄清石灰水变浑浊,实验记录如下所示:
实验操作 | 实验现象 | 实验结论及化学方程式 |
取少量滤渣B于试管中,加入足量稀盐酸,将生成的气体通入澄清的石灰水中 | ①固体全部溶解,溶液由无色变成黄色 ②澄清石灰水变浑浊 | 结论:滤渣B中有 Fe2O3,CaCO3.实验操作中反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O或CaCO3+2HCl═CaCl2+H2O+CO2↑或CO2 +Ca(OH)2 ==CaCO3↓+ H2O |
乙组:取少量滤液C于试管中,加入过量BaCl2溶液,静置,向上层清液中滴加无色配酞试液,振荡,产生白色沉淀,氯化钡与碳酸钠反应生成碳酸钡沉淀和氯化钠,氢氧化钠呈碱性,能使酚酞变红,氯化钡溶液呈中性,说明溶液中含有碳酸钠和氢氧化钠,实验记录如下所示:
实验操作 | 实验现象 | 实验结论 |
取少量滤液C于试管中,加入过量BaCl2溶液,静置,向上层清液中滴加无色酚酞试液,振荡 | ①有白色沉淀生成 ②酚酞试液由无色变成红色 | 滤液C中有NaOH、Na2CO3 |
解释与结论:
(1)碳酸钠溶液呈碱性,对氢氧化钠的检验有干扰。乙组同学实验中加入过量BaCl2溶液的目的是使碳酸钠完全反应,以防止对检验氢氧化钠产生影响;
(2)通过以上实验探究可知,磁铁能够吸引黑色粉末,铁能被磁铁吸引,说明固体中含有铁,氧化钙与水反应放热、氢氧化钠固体溶于水放热。加入水溶解时不放热,说明固体中不含有氧化钙和氢氧化钠,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,该固体样品中不一定含有碳酸钙,能确定一定含有的成分是Fe、Fe2O3、Ca(OH)2、Na2CO3。

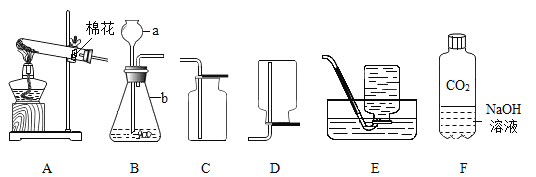
【题目】下列实验的现象或结论不正确的一组是
选项 | A | B | C | D |
实验 |
|
|
|
|
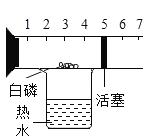
实验现象 | 打开汽水瓶盖时,汽水会自动喷出来 | 硫在空气中燃烧发出微弱的淡蓝色火 焰,硫在氧气中燃 烧发出明亮的蓝紫 色火焰 | 白磷燃烧产生大量烟,活塞先向右 再向左移动,冷却 至室温后,最终停 在刻度“4”附近 | 装铁丝的试管中有气泡产生,装铜丝 的试管中无明显现 象 |
实验结论 | 说明气体在水中的溶解度随压强的增 大而减小 | 说明氧气的浓度是影响硫燃烧剧烈程 度的因素 | 氧气约占空气体积的五分之一 | 说明铁与铜的活泼性 Fe>Cu |
A. A B. B C. C D. D
【题目】某化学兴趣小组设计了如下实验来探究影响锌与稀硫酸反应速率的因素(实验过程中杂质不能与稀硫酸反应),实验数据记录如下表:
实验编号 | 试剂 | 产生50mL氢气 的时间/s | ||
不同纯度的锌 | 稀硫酸的浓度 | 稀硫酸的用量/ mL | ||
a | 纯锌 | 30% | 30 | 52 |
b | 含杂质的锌 | 30% | 30 | 47 |
c | 纯锌 | 20% | 30 | 68 |
d | 纯锌 | 30% | 40 | 50 |
(1)实验_____和实验______(填实验编号)的实验目的是为了研究硫酸浓度对反应速率的影响。
(2)对比实验a和实验b,可以得到的实验结论是____________________。
(3)计算9.8g纯硫酸与足量的锌完全反应,可制得氢气是_________克?请你帮他们完善计算过程:
①______________②____________________