题目内容
甲、乙两烧杯中分别盛有等体积、等溶质质量分数的H2SO4溶液.现向甲杯中加入m克Mg,向乙杯中加入m克Zn,充分反应后,有一只烧杯中仍有金属未溶解,则甲、乙烧杯中原有H2SO4的溶质质量x应为( )
A.  ≤x<
≤x<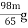 B.
B.  >x≥
>x≥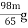
C. 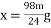 D. x<
D. x<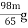
某同学将氢氧化钠溶液滴入到一定量的稀氯化铜溶液中,出现蓝绿色不溶于水的固体。该同学对生成蓝绿色而不是蓝色固体的现象产生疑惑。
(查阅资料)
(1)CuCl2溶液与NaOH溶液反应可生成蓝色固体(Cu(OH)2),在氢氧化钠较少的情况下会生成蓝绿色碱式氯化铜(Cux(OH)yClz),其不溶于水,能与酸反应。
(2)Cu(OH)2在60℃开始分解生成两种氧化物,100℃分解完全。碱式氯化铜在300℃开始分解生成氧化铜、水和氯化氢,在400℃分解完全。
(猜测)蓝绿色固体可能是:①Cu(OH)2;②Cux(OH)yClz晶体;③___。
猜想①的理由是:___(用化学方程式表示)。
(实验)该同学取31.25g蓝绿色固体,加热至100℃出现黑色固体。则猜想___不正确。继续加热到400℃至质量不再改变,并使产生的气体全部缓缓通过如图___(选填“甲”或“乙”)装置(装置中药品足量)。
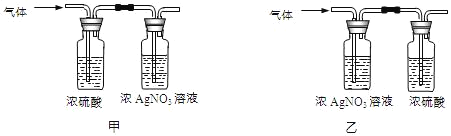
实验数据:①最终得到剩余固体24.00g;
②与硝酸银溶液反应得到的沉淀经过滤、洗涤和低温烘干,得到固体14.35g;
加热前 | 100℃ | 400℃ |
250.00g | 251.80g | 253.60g |
③浓硫酸装置中数据如表。
(延伸)
(1)碱式氯化铜常作为动物饲料的添加剂,则该碱式氯化铜与胃液发生反应的化学方程式为___。
(2)为使实验中生成蓝色固体,少出现蓝绿色固体,应作___改进(选填序号)。
a.实验中将氯化铜溶液滴加到氢氧化钠溶液中
b.实验中应提供足量、较浓的氢氧化钠溶液
c.实验应该在80℃的水浴中进行
下列事实的微观解释合理的是( )
选项 | 事实 | 微观解释 |
A | 蔗糖溶液不能导电 | 溶液中没有自由移动的粒子 |
B | 工业上用空气制取氧气的过程属于物理变化 | 分子的种类没有发生变化 |
C | 通过气味辨别醋和水 | 分子做永不停息运动 |
D | 金刚石和石墨物理性质不同 | 分子的排列方式不同 |
A. A B. B C. C D. D


