题目内容
【题目】通过化学学习,你已经掌握了实验室制取气体的有关知识,回答问题: 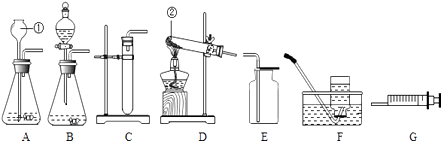
(1)请写出上图中标号仪器的名称:①;② .
(2)实验室用锌粒和稀硫酸来制取2瓶纯净的氢气时,要求能随时控制生成气体的速率并节约药品,应选用发生装置收集装置进行组合.
(3)注射器G可用于检查装置A的气密性,步骤如下:
①向锥形瓶中加入少量水至处.
②将注射器C连接到装置A的导管口处.
③缓慢拉动注射器G的活塞,观察到 , 表示装置A的气密性良好.
【答案】
(1)长颈漏斗;试管
(2)B;F
(3)浸没长颈漏斗末端;有气泡产生
【解析】解:(1)据图可以看出,①是长颈漏斗,②是试管,故填:长颈漏斗;试管.(2)实验室用锌粒和稀硫酸来制取2瓶纯净的氢气时,要求能随时控制生成气体的速率并节约药品,B装置中的分液漏斗能随时控制生成气体的速率并节约药品,故应选用发生装置是B,收集纯净的氢气应该使用的是排水法,故收集装置是F,故填:B,F;(3)检查装置的气密性时,
①向锥形瓶中加入少量水至浸没长颈漏斗末端处,形成液封.
②将注射器C连接到装置A的导管口处.
③缓慢拉动注射器G的活塞,观察到有气泡产生,表示装置A的气密性良好.
故填:浸没长颈漏斗末端,有气泡产生.
【考点精析】本题主要考查了检查装置的气密性和氢气的制取和检验的相关知识点,需要掌握装置气密性检查:先将导管的一端浸入水中,用手紧贴容器外壁,稍停片刻,若导管口有气泡冒出,松开手掌,导管口部有水柱上升,稍停片刻,水柱并不回落,就说明装置不漏气;氢气的实验室制法原理:Zn + H2SO4 = ZnSO4 +H2↑;Zn + 2HCl = ZnCl2 +H2↑不可用浓盐酸的原因 浓盐酸有强挥发性 ;不可用浓硫酸或硝酸的原因 浓硫酸和硝酸有强氧化性才能正确解答此题.

 教学练新同步练习系列答案
教学练新同步练习系列答案【题目】小明参观某养鱼池时,好奇地发现农民向养鱼池中撒一种叫做过氧化钙的淡黄
色固体,用来增加鱼池中的含氧量.小明刚学完氧气的实验室制法,于是他想是否可以用过氧化钙制取氧气.
【提出问题】过氧化钙是否可以用于制取氧气?
【查阅资料】部分内容如下:过氧化钙(CaO2)室温下稳定,在300℃时分解生成氧气,可作增氧剂、杀菌剂等.
【猜想与验证】
(1)小明依据
提出猜想 加热过氧化钙可制取氧气.
(2)小明联想到农民用过氧化钙增加鱼池中的含氧量,
提出猜想 过氧化钙与水反应可制取氧气.
实验装置 | 实验主要过程 |
| ①检验装置气密性; |
【实验结论】过氧化钙与水反应可得到氧气,但反应很慢.
【分析与反思】
①虽然没有快速收集到大量氧气,但由此实验现象,小明认为农民用过氧化钙作增氧剂的主要原因是 .
②小明希望对此实验进行改进,使该反应加快,你能帮他提出建议吗?你的合理建议: .
以上建议是否可行,还需进一步通过实验验证.
【题目】对下列实验指定容器中的液体,其解释没有体现液体的主要作用的是( )
A | B | C | D | |
实验装置 |
|
|
|
|
解释 | 集气瓶中水:吸收放出的热量 | 量筒中的水:通过水体积的变化得出O2体积 | 集气瓶中的水:冷却溅落融熔 | 集气瓶中的水:先将集气瓶内的空气排尽,后便于观察O2何时收集满 |
A.A
B.B
C.C
D.D