题目内容
(2006?玄武区二模)在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸,反应中溶液的温度与加入盐酸的体积变化如下:| 加入盐酸体积V/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
| 溶液温度上升(t)/℃ | 15.2 | 19.6 | 22.0 | 26.0 | 28.2 | 26.7 | 25.7 | 24.7 | 23.7 | 22.9 |
如用______mL(填“10mL”、“50mL”或“100mL”)量筒量取水时,面对刻度线,仰视读数,则所配制的溶液______10%(填“=”、“>”或“<”)
(2)试绘出溶液的温度与加入盐酸的体积之间的变化关系曲线.

(3)根据曲线讨论溶液温度变化的原因.
①加入盐酸的量在2mL~10mL之间时:______.
②加入盐酸的量在10mL~20mL之间时:______.
(4)若某同学提出“将氢氧化钠固体直接与10%盐酸反应,以探究中和反应是否放热”,此提议是否合理?为什么?
答:______.
(5)在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液滴加稀盐酸一会儿后,发现忘记了滴加指示剂,因而无法确定盐酸与氢氧化钠是否恰好完全反应.为了证明这两种物质是否恰好完全反应,从烧杯中取了少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是得出“两种物质已恰好完全中和”的结论.
①你认为此结论是否正确?______,理由是______;
②写出该中和反应的化学方程式______;
③请你另设计一个实验,探究上述烧杯中的溶液是否恰好完全中和,填写下表:
| 实验方法 | 可能观察到的现象 | 结论 |
【答案】分析:(1)①利用溶质质量=溶液质量×溶质质量分数计算配制溶液时所需氢氧化钠的质量,利用溶剂质量=溶液质量-溶质质量计算配制所需水的质量,再使用m=ρV换算出水的体积,选择量筒;一定溶质质量分数的溶液的配制步骤为:称量、溶解、装瓶;
(2)由上面的“溶液的温度与加入盐酸的体积变化”可知:可以先画出各个点,再连接各点成线;
(3)在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸:①加入盐酸的量在2-10mL之间时:考虑中和反应放出热量;②加入盐酸的量在l0-20mL之间时:考虑反应完成,过量盐酸起冷却降温作用;
(4)“将氢氧化钠固体直接与10%盐酸反应,以探究中和反应是否放热”,不合理,考虑固体氢氧化钠溶于水也要放热;
(5)氢氧化钠和盐酸反应生成氯化钠和水,酚酞试液在酸性和中性溶液中均为无色,故无法判断是否恰好完全反应,若完全反应则溶液呈中性,若不是恰好完全反应,则呈酸性,因此可以从检验反应后的溶液中是否含酸着手设计实验.
解答:解:(1)氢氧化钠的质量=100mL×1.02g/cm3×10%=10.2g;水的质量=100mL×1.02g/cm3-10.2g=90.18g,
水的体积=90.18g÷1g/cm3=90.18mL,选择100mL的量筒;其配置步骤为:称量、溶解、装瓶;
用量筒量取水时,若仰视读数,量取的水的体积偏大,根据溶质的质量分数=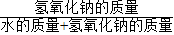
×100%,可知所配制的溶液溶质的质量分数小于10%.
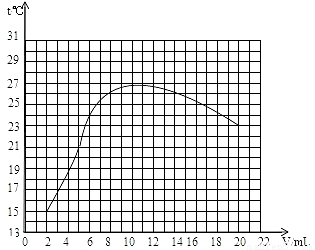
(2)根据表格中“溶液的温度与加入盐酸的体积变化”的数据,可以先画出各个点,再连接各点成线;绘出溶液的温度与加入盐酸的体积之间的变化关系曲线,见下图;
(3)在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸:①加入盐酸的量在2-10mL之间时:随盐酸量增加,中和反应放出热量增大,溶液温度上升;②加入盐酸的量在l0-20mL之间时:过量盐酸起冷却降温作用,反应停止热量散失;
(4)氢氧化钠固体又称“火碱”、“苛性钠”溶于水时放出大量的热,这样就没法确定放出的热量是中和反应放出的,还是氢氧化钠固体溶解放出的;
(5)①当加入的盐酸过量后,盐酸也不会使酚酞变色,所以结论不正确;
②)探究上述烧杯中的溶液是否恰好完全中和,可以从检验反应后的溶液中是否含酸着手设计实验,选择的试剂可以是碳酸钠,
故答案为:(1)10.2g;称量、溶解、装瓶;100,<;
(2)
(3)①随盐酸量增加,中和反应放出热量增大,溶液温度上升;②过量盐酸起冷却降温作用,反应停止热量散失;
(4)不合理,因为固体氢氧化钠溶于水也要放热;
(5)①不正确,盐酸过量后滴加酚酞,酚酞也不变色;②HCl+NaOH=NaCl+H2O;
③
点评:掌握一定溶质质量分数溶液的配置、中和反应的概念“酸碱发生的反应”及其应用;了解物质发生化学变化时的能量变化:中和放热;解答此类题的关键是正确从材料中抽取信息,准确做出判断,结合已有的知识储备并做出合理的解释.
(2)由上面的“溶液的温度与加入盐酸的体积变化”可知:可以先画出各个点,再连接各点成线;
(3)在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸:①加入盐酸的量在2-10mL之间时:考虑中和反应放出热量;②加入盐酸的量在l0-20mL之间时:考虑反应完成,过量盐酸起冷却降温作用;
(4)“将氢氧化钠固体直接与10%盐酸反应,以探究中和反应是否放热”,不合理,考虑固体氢氧化钠溶于水也要放热;
(5)氢氧化钠和盐酸反应生成氯化钠和水,酚酞试液在酸性和中性溶液中均为无色,故无法判断是否恰好完全反应,若完全反应则溶液呈中性,若不是恰好完全反应,则呈酸性,因此可以从检验反应后的溶液中是否含酸着手设计实验.
解答:解:(1)氢氧化钠的质量=100mL×1.02g/cm3×10%=10.2g;水的质量=100mL×1.02g/cm3-10.2g=90.18g,
水的体积=90.18g÷1g/cm3=90.18mL,选择100mL的量筒;其配置步骤为:称量、溶解、装瓶;
用量筒量取水时,若仰视读数,量取的水的体积偏大,根据溶质的质量分数=
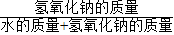
×100%,可知所配制的溶液溶质的质量分数小于10%.
(2)根据表格中“溶液的温度与加入盐酸的体积变化”的数据,可以先画出各个点,再连接各点成线;绘出溶液的温度与加入盐酸的体积之间的变化关系曲线,见下图;
(3)在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸:①加入盐酸的量在2-10mL之间时:随盐酸量增加,中和反应放出热量增大,溶液温度上升;②加入盐酸的量在l0-20mL之间时:过量盐酸起冷却降温作用,反应停止热量散失;
(4)氢氧化钠固体又称“火碱”、“苛性钠”溶于水时放出大量的热,这样就没法确定放出的热量是中和反应放出的,还是氢氧化钠固体溶解放出的;
(5)①当加入的盐酸过量后,盐酸也不会使酚酞变色,所以结论不正确;
②)探究上述烧杯中的溶液是否恰好完全中和,可以从检验反应后的溶液中是否含酸着手设计实验,选择的试剂可以是碳酸钠,
| 实验验方法 | 可能观察到的现象 | 结论 |
| 从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加碳酸钠溶液 | 1、有气泡产生 2、无气泡产生 | 1、不是恰好完全反应 2、恰好完全反应 |
(2)

(3)①随盐酸量增加,中和反应放出热量增大,溶液温度上升;②过量盐酸起冷却降温作用,反应停止热量散失;
(4)不合理,因为固体氢氧化钠溶于水也要放热;
(5)①不正确,盐酸过量后滴加酚酞,酚酞也不变色;②HCl+NaOH=NaCl+H2O;
③
| 实验验方法 | 可能观察到的现象 | 结论 |
| 从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加碳酸钠溶液 | 1、有气泡产生 2、无气泡产生 | 1、不是恰好完全反应 2、恰好完全反应 |
点评:掌握一定溶质质量分数溶液的配置、中和反应的概念“酸碱发生的反应”及其应用;了解物质发生化学变化时的能量变化:中和放热;解答此类题的关键是正确从材料中抽取信息,准确做出判断,结合已有的知识储备并做出合理的解释.

练习册系列答案
相关题目
 (2006?玄武区二模)测定黄铜屑(锌铜合金)的组成有多种方案.某学习小组用图示装置测定黄铜屑中锌的质量分数,取一定量黄铜屑放入锥形瓶中,并加入足量稀硫酸.不同时间电子天平的读数如下表所示(不考虑H2O逸出及溶液温度变化):
(2006?玄武区二模)测定黄铜屑(锌铜合金)的组成有多种方案.某学习小组用图示装置测定黄铜屑中锌的质量分数,取一定量黄铜屑放入锥形瓶中,并加入足量稀硫酸.不同时间电子天平的读数如下表所示(不考虑H2O逸出及溶液温度变化):| 反应时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | |
| 锥形瓶及所盛物质总质量/g | 335.70 | 335.54 | 335.44 | 335.38 | 335.34 | 335.32 | 335.31 | 335.30 | 335.30 |
(2)若要计算黄铜屑中锌的质量分数,还缺少的数据是______.若该数据用a表示,求黄铜屑中锌的质量分数(写出计算过程).
(3)请你再设计一个测定黄铜屑中锌的质量分数的方案.
(2006?玄武区二模)蜡烛(主要成分:石蜡)是我们生活中的常用品.让我们通过实验共同来探究它的组成及有关性质.
(1)用小刀轻轻切下一小块蜡烛,把它放入水中,发现蜡烛浮在水面上.由此你能得到的结论有①______,②______.
(2)查阅资料后得知石蜡中含有碳等元素.为了验证石蜡中含有碳元素,你将进行怎样的实验操作?试完成实验报告.
(3)我还能提出一个与蜡烛有关,需要再探究的新问题:______.
(1)用小刀轻轻切下一小块蜡烛,把它放入水中,发现蜡烛浮在水面上.由此你能得到的结论有①______,②______.
(2)查阅资料后得知石蜡中含有碳等元素.为了验证石蜡中含有碳元素,你将进行怎样的实验操作?试完成实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
石蜡中有碳元素 |
(2006?玄武区二模)合作探究:某兴趣小组将大小相同的若干块棉布在五分不同体积分数的酒精溶液中浸透后取出点火,做“烧不坏的手帕”实验.其实验结果记录如下:
推测⑤的结果.分析实验②③中“酒精烧完棉布无损”的原因,实验室里常出现酒精灯内有酒精却点不着的现象.你认为可能的原因.
| 实验序号 | ① | ② | ③ | ④ | ⑤ |
| 所用酒精的 体积分数 | 95% | 65% | 55% | 15% | 5% |
| 实验 现象 | 酒精烧完 棉布烧坏 | 酒精烧完 棉布无损 | 酒精烧完 棉布无损 | 不燃烧 |
