题目内容
【题目】小明同学打算自己探究一下MnO2在分解过氧化氢时所起的作用,但手边没有现成的MnO2药品,只有高锰酸钾,30%过氧化氢溶液、木条、水、火柴,其他仪器可任选.
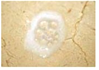
(1)若要先得到MnO2粉末,反应原理是(用化学式表示化学反应) ,装置为 (用图示).
(2)已知实验(1)中试管中剩下两种物质,其中二氧化锰难溶于水,而另一种易溶于水,小明用了一种方法将它们分离开来,步骤为:① ,② .
(3)小明认为若要探究MnO2在较低的温度下对分解H2O2有无催化作用,需作对比实验,他设计了三组实验:①在试管中加入5ml 30%的过氧化氢溶液,把带火星的木条伸入试管,看木条是否复燃.②......;③在第3支试管中加入5ml 30%过氧化氢溶液,并加入少量二氧化锰,把带火星的木条伸入试管,观察木条是否复燃.
你认为小明设计的第2组实验过程应为: .
(4)小明得到的是③中有O2放出,但他认为③中有O2放出是因为MnO2与H2O2发生了反应,你如何帮他设计实验来说明MnO2没有和H2O2起反应,而只是起了催化作用?
【答案】
(1)2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;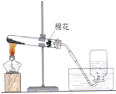 ;
;
(2)①溶解;②过滤;
(3) 在第二支试管中加入少量二氧化锰,把带火星的木条伸入试管,观察木条是否复燃;
(4) 将第三组中的二氧化锰洗净、干燥、称其质量,然后将其加入另一支试管中,向其加入过氧化氢溶液后,仍然有氧气产生,过滤得到二氧化锰,干燥、称其质量,发现其质量不变,重复上述实验,得到相同的结果.
【解析】
试题分析:(1)高锰酸钾分解的化学方程式为2KMnO4![]() K2MnO4+MnO2+O2↑;其反应装置应用固固加热制气装置,装置图为
K2MnO4+MnO2+O2↑;其反应装置应用固固加热制气装置,装置图为 ;
;
(2)因为二氧化锰难溶于水,而锰酸钾溶于水,所以可以将混合物溶解后,再过滤从而得到难溶的二氧化锰;
(3)为了排除氧气是由二氧化锰单独产生的可能,所以设计的第2组实验是在第二支试管中加入少量二氧化锰,把带火星的木条伸入试管,观察木条是否复燃;
(4)二氧化锰只起催化作用时,它的化学性质和质量在化学反应前后不会发生变化,所以只要我们验证其化学性质和质量在反应前后不变即可.所以将第三组中的二氧化锰洗净、干燥、称其质量,然后将其加入另一支试管中,向其加入过氧化氢溶液后,仍然有氧气产生,过滤得到二氧化锰,干燥、称其质量,发现其质量不变,重复上述实验,得到相同的结果,由此得出二氧化锰只起了催化作用.

 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
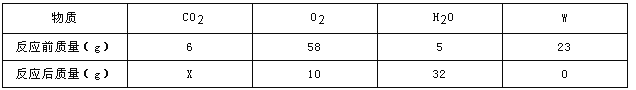
课堂练加测系列答案【题目】一定条件下,在一个密闭器内发生某反应,测得反应前后各物质的质量如下表所示,下列说法正确的是
物质 | CO2 | O2 | H2O | W |
反应前质量(g) | 6 | 58 | 5 | 23 |
反应后质量(g) | X | 10 | 32 | 0 |
A.该反应属于化合反应
B.W是一种由碳、氢两种元素组成的化合物
C.W是一种由碳、氢、氧三种元素组成的化合物
D.X的值为44