题目内容
【题目】某兴趣小组在相同条件下,将10.00g下列物质分别置于相同规格的烧杯,并敞口存放于空气中,烧杯中物质质量随时间变化如下表,回答下列问题。
时间 | 质量/g | |||||
水 | 饱和石灰水 | 稀盐酸 | 浓硫酸 | 氢氧化钠浓溶液 | 氯化钙溶液 | |
1天 | 8.16 | 8.37 | 8.64 | 11.18 | 9.38 | 10.25 |
2天 | 5.76 | 5.94 | 6.69 | 12.55 | 8.47 | 10.33 |
(1)下列图示能反映水在空气中放置时发生变化的微观示意图是_________(填字母序号)。图中表示氧原子,表示氢原子)

(2)石灰水在空气中久置后有浑浊现象,写出该反应的化学方程式___________________。
(3)为研制一种安全、环保的除湿剂,可选择上表中的__________________(填溶质的化学式)。
(4)将10.00g氯化钠浓溶液敞口久置后,最终得到2.26g晶体,则该溶液是________(填“饱和”或“不饱和”)溶液。(已知该温度下氯化钠溶解度为36.1g)
(5)为进一步研究稀盐酸敞口久置后浓度变化,该小组开展如下探究。
①甲同学猜想浓度可能会变大,理由是_______________________。
②为验证甲同学的猜想是否正确,设计实验方案:_________________________。
(注意:若答对第(6)小题奖励4分,化学试卷总分不超过60分。)
(3)乙同学取20%的氢氧化钠溶液20.00g,敞口放置一段时间后部分变质,得到18.80g溶液,由此能否计算所得溶液中溶质组成?若能,请计算其组成;若不能,请补充完成实验方案设计,同时说明需要测定的数据(用a表示),并计算a的取值范围___________。(不要求写出计算过程)
【答案】 D Ca(OH)2+CO2=CaCO3↓ + H2O CaCl2 不饱和 稀盐酸中水的蒸发量大于HCl的挥发量 取等质量的原盐酸和久置的盐酸,均加酚酞溶液,分别滴入等浓度的NaOH溶液,至溶液由无色变红色时,比较消耗氢氧化钠的量(其他合理答案均给分) 不能。实验方案:将变质后溶液加热蒸干,称量所得固体质量为ag。a的取值范围:4.00<a<5.30。(本小题为开放性试题,其他合理答案均给分)
【解析】(1)水放置在空气中时表面的水分子会扩散到空气中,故选D;
(2)石灰水在空气中久置后有浑浊现象是由于氢氧化钙与空气中的二氧化碳反应生成碳酸钙沉淀和水,反应方程式为Ca(OH)2+CO2=CaCO3↓ + H2O;
(3)氯化钙溶液和浓硫酸溶液的质量增加,但是浓硫酸有强烈的腐蚀性,故选氯化钙溶液;
(4)该温度下氯化钠溶解度为36.1g,则该温度下10g浓溶液中最多能溶解氯化钠的质量为![]() ,故该溶液是不饱和溶液;
,故该溶液是不饱和溶液;
(5)①甲同学猜想浓度可能会变大,理由是稀盐酸敞口放置后有水分蒸发。
②为验证甲同学的猜想是否正确,设计实验方案:取等质量的原盐酸和久置的盐酸,均加酚酞溶液,分别滴入等浓度的NaOH溶液,至溶液由无色变红色时,比较消耗氢氧化钠的量;
(6)不能确定;实验方案:将变质后溶液加热蒸干,称量所得固体质量为ag。当没有变质时,蒸干后固体的质量为20g![]() =4g,设质量为4g的氢氧化钠完全变质后生成碳酸钠的质量为x
=4g,设质量为4g的氢氧化钠完全变质后生成碳酸钠的质量为x
2NaOH+CO2===Na2CO3+H2O
80 106
4.00g x
![]() =
=![]() ,解得x=5.30g,
,解得x=5.30g,
故a的取值范围:4.00<a<5.30

 阅读快车系列答案
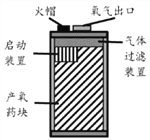
阅读快车系列答案【题目】某化学兴趣小组同学对家用普通干电池中含有的物质产生了浓厚的兴趣。他们剥开电池时闻到氨味且发现有黑色物质。
(提出问题)为什么有氨味?黑色物质的成分是什么?
(猜想假设)能闻到氨味说明含有铵盐(如NH4Cl);黑色固体可能有铁粉、氧化铜或二氧化锰。
(实验探究)同学们分别设计实验进行探究。
实验I.小聪取适量黑色物质与______________混合置于研钵内研磨,嗅到强烈氨味,再用湿润的红色石蕊试纸检测,观察到试纸变蓝,证明黑色物质中含有铵盐。
实验II.小敏将黑色物质加入适量的水中搅拌溶解,静置后______,取不溶物进行实验。
实验步骤 | 实验现象 | 实验结论 |
1.取适量黑色滤渣装入试管中,再加入过量稀盐酸 | 无气泡生成,溶液不变色 | ________________ |
2.取适量黑色滤渣装入另一支试管中,再加入______溶液,向上述试管中伸入带火星的小木条。 | _________________ | 黑色粉末中含有二氧化锰 |
(交流讨论)步骤2中发生反应的化学方程式为______________。