题目内容
相同质量、等质量分数的四份稀盐酸,分别与:①Mg ②MgO③Mg(OH)2④MgCO3恰好完全反应得无色澄清溶液,则所得溶液中MgCl2的质量分数大小关系的比较下列正确的是( )
| A、①=②=③=④ |
| B、①>②>③>④ |
| C、①>②=④>③ |
| D、④>③>②>① |
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:根据化学变化前后元素质量不变,可知消耗质量和质量分数均相同的稀盐酸时,①Mg、②MgCO3、③Mg(OH)2、④Mg0四种物质恰好完全反应完全后(反应物均完全反应)生成氯化镁质量相等,即反应后所得溶液中溶质质量相等;因此,为比较所得溶液中溶质质量分数大小,只需要考虑反应后溶液的质量的变化即可完成比较.
解答:解:根据反应的化学方程式,可判断与等质量的盐酸恰好完全反应后溶液质量的增加值为:
Mg+2HCl═MgCl2+H2↑ 溶液质量增加
24 73 95 2 24-2=22
MgCO3+2HCl=MgCl2+H2O+CO2↑溶液质量增加
84 73 95 18 44 84-44=40
Mg(OH)22HCl+=MgCl2+2H2O 溶液质量增加
58 73 95 36 58
MgO+2HCl=MgCl2+H2O 溶液质量增加
40 73 95 18 40
根据反应后溶液溶液量,与镁反应时溶液增加量最小,即与镁恰好完全反应时所得溶液的质量最小,而反应后所得溶质氯化镁的质量相同,因此,与镁反应后所得溶液的溶质质量分数最大;同理分析可得与氢氧化镁反应后所得溶液的溶质质量分数最小;氧化镁和碳酸镁分别与等质量的盐酸恰好完全反应后溶液的溶质质量分数相等.
答案:C
Mg+2HCl═MgCl2+H2↑ 溶液质量增加
24 73 95 2 24-2=22
MgCO3+2HCl=MgCl2+H2O+CO2↑溶液质量增加
84 73 95 18 44 84-44=40
Mg(OH)22HCl+=MgCl2+2H2O 溶液质量增加
58 73 95 36 58
MgO+2HCl=MgCl2+H2O 溶液质量增加
40 73 95 18 40
根据反应后溶液溶液量,与镁反应时溶液增加量最小,即与镁恰好完全反应时所得溶液的质量最小,而反应后所得溶质氯化镁的质量相同,因此,与镁反应后所得溶液的溶质质量分数最大;同理分析可得与氢氧化镁反应后所得溶液的溶质质量分数最小;氧化镁和碳酸镁分别与等质量的盐酸恰好完全反应后溶液的溶质质量分数相等.
答案:C
点评:本题的解决技巧在于利用化学变化前后元素质量不变,判断出反应后所得溶液中溶质质量相等,然后计算反应后溶液的质量,这使得本题的解答简便很多.

练习册系列答案
相关题目
下列可以做食品中干燥剂的是( )
| A、氧化钙 | B、浓硫酸 |
| C、氢氧化钠 | D、碱石灰 |
下列物质的用途主要由物质的物理性质决定的是( )
| A、氮气用作食品包装袋内的保护气 |
| B、小苏打用于治疗胃酸过多 |
| C、铜用于制作电线 |
| D、镁粉用于制作照明弹 |
下列对有关实验现象的描述正确的是( )
| A、铁丝在空气中燃烧时,火星四射,有黑色物质生成 |
| B、红热木炭放入盛有氧气的集气瓶中,剧烈燃烧,产生白光 |
| C、石蜡在空气中燃烧时,有水和二氧化碳生成 |
| D、铁钉浸到硫酸铜溶液中,溶液逐渐变成浅绿色 |
测得某物质中只含有碳元素,这种物质( )
| A、一定是纯净物 |
| B、一定是混合物 |
| C、可能是纯净物也可能是混合物 |
| D、可能是化合物 |
量取8mL水稀释浓硫酸的下列操作错误的是( )
A、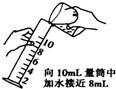 |
B、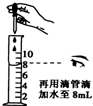 |
C、 |
D、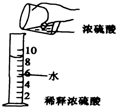 |
可与烧瓶、试管、蒸发皿归为一类的是( )
| A、量筒 | B、漏斗 | C、集气瓶 | D、烧杯 |
人体是元素的仓库,其中含量最大的元素是( )
| A、H | B、C | C、O | D、Ca |
