题目内容
下列实验方案中,合理的是( )
| A、要检验混合气体中含有CO和CO2:先将气体通过灼热氧化铜,再通过澄清石灰水 |
| B、要除去BaSO4中的BaCO3:取样,加足量稀盐酸,过滤,洗涤,干燥 |
| C、要区分NaOH和Na2CO3两种白色固体:取样,加入足量水,观察 |
| D、要分离氯化钙和碳酸钠:先加入足量水,然后过滤,蒸发 |
考点:化学实验方案设计与评价,混合物的分离方法,常见气体的检验与除杂方法,盐的化学性质,酸、碱、盐的鉴别
专题:简单实验方案的设计与评价
分析:A、根据一氧化碳和氧化铜反应生成二氧化碳气体进行解答;
B、根据碳酸钡和盐酸反应生成氯化钡、水和二氧化碳,而硫酸钡不和盐酸反应进行解答;
C、根据氢氧化钠固体和碳酸钠固体溶于水都放热进行解答;
D、根据氯化钙和碳酸钠溶于水后会反应生成碳酸钙沉淀和氯化钠进行解答.
B、根据碳酸钡和盐酸反应生成氯化钡、水和二氧化碳,而硫酸钡不和盐酸反应进行解答;
C、根据氢氧化钠固体和碳酸钠固体溶于水都放热进行解答;
D、根据氯化钙和碳酸钠溶于水后会反应生成碳酸钙沉淀和氯化钠进行解答.
解答:解:A、一氧化碳和氧化铜反应生成二氧化碳气体,所以不能用先将气体通过灼热氧化铜,再通过澄清石灰水的方法检验混合气体中含有CO和CO2,故A错误;
B、BaCO3能与足量稀盐酸反应生成氯化钡、水和二氧化碳,硫酸钡不能与稀盐酸反应,且难溶于水,再过滤、洗涤、干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故B正确;
C、氢氧化钠固体和碳酸钠固体溶于水都放热,所以不可用加入足量水,观察温度变化的方法区分NaOH和Na2CO3,故C错误;
D、氯化钙和碳酸钠溶于水后会反应生成碳酸钙沉淀和氯化钠,所以不能用加入足量水,然后过滤,蒸发的方法分离氯化钙和碳酸钠,故D错误.
故选:B.
B、BaCO3能与足量稀盐酸反应生成氯化钡、水和二氧化碳,硫酸钡不能与稀盐酸反应,且难溶于水,再过滤、洗涤、干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故B正确;
C、氢氧化钠固体和碳酸钠固体溶于水都放热,所以不可用加入足量水,观察温度变化的方法区分NaOH和Na2CO3,故C错误;
D、氯化钙和碳酸钠溶于水后会反应生成碳酸钙沉淀和氯化钠,所以不能用加入足量水,然后过滤,蒸发的方法分离氯化钙和碳酸钠,故D错误.
故选:B.
点评:物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
只用一种试剂区别NaNO3、AgNO3、Na2CO3三种无色溶液,可选用( )
| A、CaCl2溶液 |
| B、盐酸 |
| C、稀硝酸 |
| D、氯化钠溶液 |
下列物质间的转化不能一步实现的是( )
| A、NaHCO3-CO2 |
| B、CO2-CaCO3 |
| C、CaO-Cacl2 |
| D、KNO3-K2CO3 |
下列化学方程式书写正确的是( )
A、4P+5O2
| ||||
| B、2Fe+6HCl═2FeCl3+3H2↑ | ||||
| C、Fe+CuCl2═FeCl2+Cu↓ | ||||
| D、KMnO4═K2MnO4+MnO2+O2↑ |
实验室现有如图所示的仪器装置.某同学准备用这些仪器装置及相关试剂制取气体,下列有关说法正确的是( )
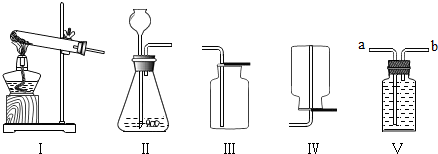

| A、用氯酸钾制取氧气与用过氧化氢溶液制取氧气反应条件相同 |
| B、实验制取氧气和二氧化碳的发生装置都可以选择Ⅱ |
| C、适合于Ⅲ或Ⅳ收集的气体一定溶于水 |
| D、用Ⅴ收集二氧化碳时,应从导管b通入二氧化碳(瓶内装水) |
生活中的下列现象,只发生物理变化的是( )
| A、汽油挥发 | B、甲烷燃烧 |
| C、铜器生锈 | D、苹果腐烂 |
下列各组化合物中,前者是离子化合物,后者是共价化合物的一组是( )
| A、NaCl,CaCl2 |
| B、HCl,KCl |
| C、CO2,H2O |
| D、ZnSO4,NH3 |
把黑色粉末加强热后,有红色物质生成,同时产生一种能使澄清石灰水变浑浊的气体,则该黑色粉末是( )
| A、木炭粉和MnO2 |
| B、CuO |
| C、木炭粉和CuO |
| D、木炭粉 |