题目内容
为减少水污染,实验结束时,同学们利用课余时间处理含有CuSO4、ZnSO4、FeSO4的废液,回收工业重要原料硫酸锌和有关金属.有关资料:
| 物质名称 | 氢氧化钙 | 氢氧化铜 | 氢氧化铁 | 氢氧化锌 | 硫酸钡 | 硫酸钙 |
| 溶解性 | 微溶 | 难溶 | 难溶 | 难溶 | 难溶 | 微溶 |
请回答:
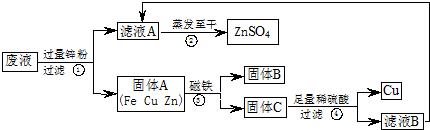
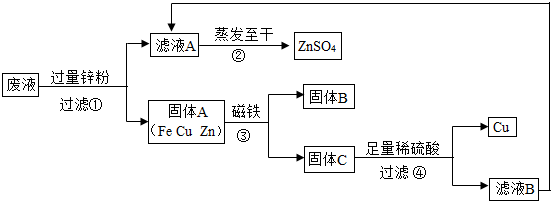
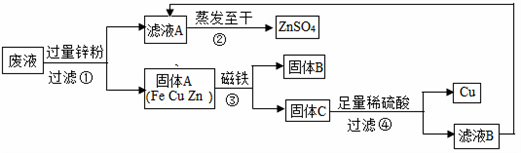
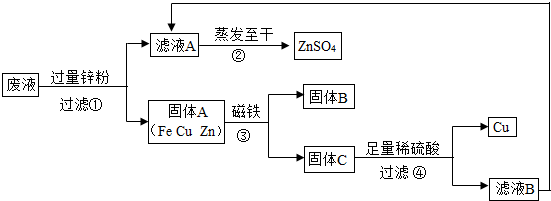
(1)滤液A和滤液B含有相同的溶质,其名称是________.
(2)写出步骤①其中一个反应的化学方程式________.
(3)步骤①加入的锌粉为什么要过量,请简要说理由________.
(4)要检验步骤④中加入的稀硫酸是否足量的方法是________.
解:(1)废液中含有硫酸铜、硫酸锌和硫酸亚铁,加入的过量锌粉与硫酸铜和硫酸亚铁反应生成硫酸锌,剩余的锌与硫酸反应生成硫酸锌,所以本题答案为:硫酸锌;
(2)锌排在铁和铜的前面,能与废液中的硫酸铜和硫酸亚铁反应生成硫酸锌,同时生成相应的金属铜和铁,所以本题答案为:Zn+CuSO4=ZnSO4+Cu;
(3)为充分回收硫酸锌和金属铁与铜,需加入过量的锌粉充分反应,所以本题答案为:确保废液中的铁离子和铜离子完全反应;
(4)铁能被磁铁吸引,故C中含有的是锌和铜,锌可以与硫酸反应生成氢气,若有锌剩余则加酸会产生气泡,说明酸量不足,所以本题答案为:取步骤④的滤渣于试管中加入少量稀硫酸,若有气泡产生则酸不足量(或若无气泡产生,则酸已足量).
分析:在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,氢前的金属能与酸发生置换反应生成氢气,可以根据金属与酸的反应和金属与盐溶液的反应来进行金属混合物的分离.
点评:本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.
(2)锌排在铁和铜的前面,能与废液中的硫酸铜和硫酸亚铁反应生成硫酸锌,同时生成相应的金属铜和铁,所以本题答案为:Zn+CuSO4=ZnSO4+Cu;
(3)为充分回收硫酸锌和金属铁与铜,需加入过量的锌粉充分反应,所以本题答案为:确保废液中的铁离子和铜离子完全反应;
(4)铁能被磁铁吸引,故C中含有的是锌和铜,锌可以与硫酸反应生成氢气,若有锌剩余则加酸会产生气泡,说明酸量不足,所以本题答案为:取步骤④的滤渣于试管中加入少量稀硫酸,若有气泡产生则酸不足量(或若无气泡产生,则酸已足量).
分析:在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,氢前的金属能与酸发生置换反应生成氢气,可以根据金属与酸的反应和金属与盐溶液的反应来进行金属混合物的分离.
点评:本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目
为减少水污染,实验结束时,同学们利用课余时间处理含有CuSO4、ZnSO4、FeSO4的废液,回收工业重要原料硫酸锌和有关金属.(资料卡):
| 物质名称 | 氢氧化钙 | 氢氧化铜 | 氢氧化铁 | 氢氧化锌 | 硫酸钡 | 硫酸钙 |
| 溶解性 | 微溶 | 难溶 | 难溶 | 难溶 | 难溶 | 微溶 |

请回答:
(1)滤液A和滤液B含有相同的溶质,其名称是______.
(2)写出步骤①其中一个反应的化学方程式______.
(3)步骤①加入的锌粉为什么要过量,请简要说理由______.
(4)要检验步骤④中加入的稀硫酸是否足量的方法是______.
(5)若在废液缸里加入适量氢氧化钙也能达到污水的排放标准,这主要是将对环境有害的重金属离子从可溶性盐转变为______,如果加入氢氧化钙的量恰好,此时的废液中除水外还有______种物质,试写出生成物中属于盐类的物质的化学式______.