题目内容
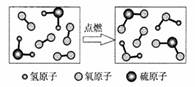
(6分)在“宏观-微观-符号”之间建立联系,是化学学科特有的思维方式。图中
 表示碳原子、
表示碳原子、 表示氧原子、
表示氧原子、 表示氢原子。
表示氢原子。
(1)水煤气是一种重要的气体燃料,以下是生产水煤气反应的微观过程示意图:
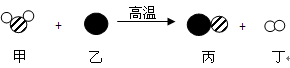
①甲、乙、丙、丁中属于氧化物的是 (填代号)。
②甲中,氢、氧元素的质量比为 。
③该反应的基本反应类型为 。
(2)在一密闭容器内有A、B两种物质各96 g组成的混合物,在一定条件下发生化学反应,反应后容器中有88 g C、36 g D和若干B。A、C、D三种物质的微观示意图如表所示:

①反应后容器中剩余物质B的质量为 g。
②已知:B的相对分子质量为28。请补全该反应的化学方程式:
O2 + 一定条件2CO2 + 2H2O
 表示碳原子、
表示碳原子、 表示氧原子、
表示氧原子、 表示氢原子。
表示氢原子。(1)水煤气是一种重要的气体燃料,以下是生产水煤气反应的微观过程示意图:

①甲、乙、丙、丁中属于氧化物的是 (填代号)。
②甲中,氢、氧元素的质量比为 。
③该反应的基本反应类型为 。
(2)在一密闭容器内有A、B两种物质各96 g组成的混合物,在一定条件下发生化学反应,反应后容器中有88 g C、36 g D和若干B。A、C、D三种物质的微观示意图如表所示:

①反应后容器中剩余物质B的质量为 g。
②已知:B的相对分子质量为28。请补全该反应的化学方程式:
O2 + 一定条件2CO2 + 2H2O
(1)①甲、丙(填化学式等合理答案均可得分)
② 1:8
③ 置换反应
(2)① 68
② 3 C2H4
② 1:8
③ 置换反应
(2)① 68
② 3 C2H4
试题分析:(1)根据微粒的微观模拟示意图可知,甲为H2O,乙为C,丙为CO,丁为H2;故该反应的化学方程式为H2O+C=CO↑+H2↑。
① 甲(H2O)是由H、O两种元素组成的纯净物,故属于氧化物;
乙(C)是由C元素组成的纯净物,故属于单质;
丙(CO)是由C、O两种元素组成的纯净物,故属于氧化物;
丁(H2)是由H元素组成的纯净物,故属于单质。故属于氧化物的是甲、丙。
② 甲(H2O)中,氢、氧元素的质量比=(1×2):16=1:8。
③ 根据反应的化学方程式H2O+C=CO↑+H2↑,可知该反应的反应物和生成物都是一种单质和一种化合物,故其基本反应类型为置换反应。
(2)根据反应前后物质的质量变化关系可知,反应后C、D的质量增大,则为反应的生成物,且C、D增大的质量分别为88g和36g,即生成物总质量为88g+36g=124g;而A、B的质量减小,则为反应的反应物,且A减小的质量为96g(反应后没有A剩余),即参加反应的A的质量为96g;根据质量守恒定律可知,B为反应物,且参加反应的B的质量为124g-96g=28g,则①反应后物质B的质量为96g-28g=68g;
②根据微粒的微观模拟示意图可知,D为H2O,C为CO2,A为O2;设化学方程式中O2的计量数为x,则可根据氧气与二氧化碳的实际质量之比,求出x。
xO2 + 一定条件2CO2 + 2H2O
32x 88
96g 88g
32x:88=96g:88g
解得x=3
由此可知,化学方程式左边有O原子6个,而化学方程式右边有O原子6个,C原子2个和H原子4个,根据化学反应过程中,原子的种类和数目都不变可知,B中含有C原子2个和H原子4个,且结合题意“B的相对分子质量为28”可知,B为C2H4。
点评:分子是由原子构成的,且同种原子构成的分子是单质分子,不同种原子构成的分子是化合物分子。试题通过给出微粒的模型,考查学生的观察能力和对基本概念的理解与运用能力,以检测考生从微观角度认识化学的意识和能力。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目