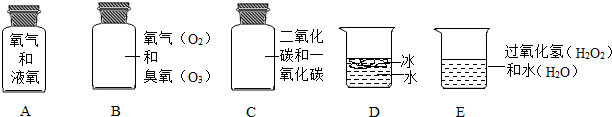
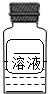
题目内容
 如图表示一瓶硫酸亚铁溶液,请按要求填写化学符号:
如图表示一瓶硫酸亚铁溶液,请按要求填写化学符号:(1)其溶液中阳离子的符号
(2)溶剂水中氢元素的化合价
(3)在如图标签的横线上填写硫酸亚铁的化学式
分析:首先要熟记常见元素与常见原子团的化合价以及化合价的规律和原则,弄清化合价与离子表示方法上的异同点(两同:数值和正负号,两不同:位置和顺序)和化合价数值交叉法书写化学式(即将正、负化合价的数值交叉到相应符号的右下角,但注意原子团看作一体,含约数的一般要约分);然后,分析出硫酸亚铁溶液中,溶质是硫酸亚铁,溶剂是水;再顺藤摸瓜即可.
(1)硫酸亚铁是由亚铁离子和硫酸根离子构成的.根据离子符号的书写方法(在元素符号的右上角标出所带的电荷数和电性),不难写出亚铁离子Fe2+和硫酸根离子SO42-.
(2)根据化合价的原则(在化合物中正、负化合价的代数和为零)和水中的氧元素的化合价为-2价,就可求出其中的氢元素的化合价+1价,并将其标注在氢元素符号的正上方.
(3)根据化学式的书写方法和构成硫酸亚铁的亚铁离子和硫酸根离子的化合价+2价、-2价,可得其化学式为FeSO4
(1)硫酸亚铁是由亚铁离子和硫酸根离子构成的.根据离子符号的书写方法(在元素符号的右上角标出所带的电荷数和电性),不难写出亚铁离子Fe2+和硫酸根离子SO42-.
(2)根据化合价的原则(在化合物中正、负化合价的代数和为零)和水中的氧元素的化合价为-2价,就可求出其中的氢元素的化合价+1价,并将其标注在氢元素符号的正上方.
(3)根据化学式的书写方法和构成硫酸亚铁的亚铁离子和硫酸根离子的化合价+2价、-2价,可得其化学式为FeSO4
解答:答:(1)根据离子符号的书写方法,硫酸亚铁溶液中阳离子(亚铁离子)的符号为 Fe2+;阴离子(硫酸根离子)的符号为 SO42-;
(2)根据化合价的原则,以及水中的氧元素的化合价为-2价,就可求出其中的氢元素的化合价+1价,即
2O.
(3)根据化学式的书写方法和构成硫酸亚铁的亚铁离子和硫酸根离子的化合价+2价、-2价,即可在试剂瓶的标签的横线上填写出硫酸亚铁的化学式.故答案为:FeSO4.
(2)根据化合价的原则,以及水中的氧元素的化合价为-2价,就可求出其中的氢元素的化合价+1价,即
| +1 |
| H |
(3)根据化学式的书写方法和构成硫酸亚铁的亚铁离子和硫酸根离子的化合价+2价、-2价,即可在试剂瓶的标签的横线上填写出硫酸亚铁的化学式.故答案为:FeSO4.
点评:本题既考查了化合价与离子表示方法上的异同点,又考查了常见元素与常见原子团的化合价以及化合价的规律和原则,还考查了化学式的书写方法和技巧.这类题几乎是在所有类型化学试题中,都会出现.要想做好此类题,就必须要弄清这些最基础、最重要的东西;也就是,要落实好“双基”(基础知识和基本技能).只有这样答题时,才能沉着应战、正确解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
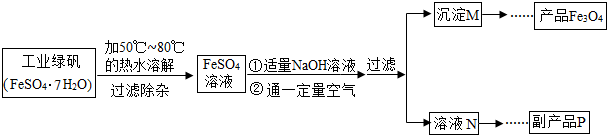
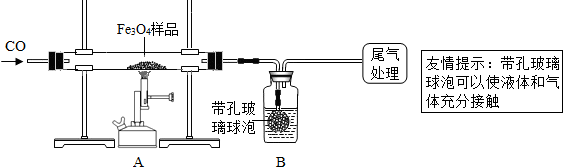
 如图表示一瓶硫酸亚铁溶液,请按要求填写化学符号:
如图表示一瓶硫酸亚铁溶液,请按要求填写化学符号: