题目内容
【题目】科技节活动中,化学实验小组做了如下实验,请回答以下问题。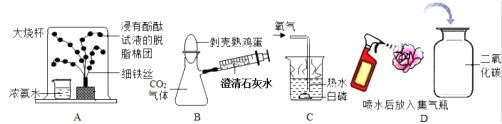
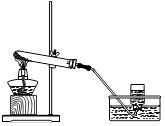
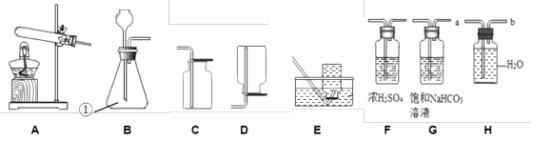
(1)图 A 实验可观察到“铁树”上浸有无色酚酞试液的棉团由白色变为色,该实验中没有涉及的性质是(填字母)。
A.氨分子是不断运动的 B.氨分子有一定质量 C.浓氨水具有挥发性
(2)图B实验,将注射器中澄清石灰水注入瓶中,会看到鸡蛋被“吞”入瓶中,该实验中涉及的化学方程式为。
(3)图 C 实验,当通过导管向热水中通入氧气时,白磷在水下燃烧,该实验说明燃烧需要的条件为:①可燃物;②温度达到燃烧所需要的;③ , 反应的化学方程式为。
(4)图D实验观察到紫色小花变为红色,小花变红的原因是(用化学方程式表示)。
【答案】
(1)红;B
(2)CO2 + Ca(OH)2 = CaCO3↓+ H2O
(3)着火点;氧气;4P+5O2![]() 2P2O5
2P2O5
(4)CO2+ H2O═ H2CO3
【解析】解:(1)氨水具有挥发性,是因为氨分子在不断的运动,氨水具有碱性,能使酚酞试液变红;(2)二氧化碳与氢氧化钙溶液反应生成碳酸钙沉淀和水,气体被消耗,导致瓶内的压强变小,从而鸡蛋被吸入瓶中,化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;(3)当通过导管向热水中通入氧气时,白磷在水下燃烧,说明燃烧还需要可燃物与氧气接触;(4)二氧化碳能与水反应生成碳酸,碳酸能使石蕊变红,化学方程式为:H2O+CO2=H2CO3 .
故答案为:(1)红,B;(2)Ca(OH)2+CO2═CaCO3↓+H2O;(3)可燃物与氧气接触;(4)H2O+CO2=H2CO3 .
根据已有的知识进行分析,碱性物质能使酚酞试液变红;二氧化碳能与氢氧化钙反应,导致瓶内的压强变小;根据燃烧的条件进行回答;二氧化碳的水溶液呈酸性,能使石蕊试液变红.

 互动英语系列答案
互动英语系列答案【题目】如图所示,某兴趣小组在进行酸碱中和反应的实验探究时,向烧杯中氢氧化钠溶液中滴加稀盐酸一会儿后,发现忘记滴加指示剂.
(1)甲同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色. 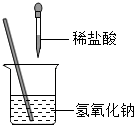
请写出该中和反应方程式: .
(2)猜想与假设: 【猜想一】甲同学:“两种物质已恰好完全中和,溶液呈中性”;
【猜想二】乙同学:“反应后氢氧化钠过量,溶液呈碱性”;
【猜想三】丙同学: .
甲、丙两位同学经过讨论后觉得乙同学的猜想不正确,两位同学的理由是:
(3)设计并进行实验: ①为了验证自己的猜想,甲同学设计了以下实验方案:
实验步骤 | 实验现象 | 实验结论 |
用洁净干燥的玻璃棒蘸取少量反应后的溶液滴在干燥的pH试纸上,观察颜色变化并与标准比色卡对比. | pH(填“>”、“=”或“<”)7 | 猜想一不成立 |
②请你设计另一个实验(与甲同学方案不同)方案,验证丙同学的猜想,并填写下表:
实验步骤 | 实验现象 | 实验结论 |
猜想三: |