题目内容
铝热反应常用于冶炼或焊接金属,反应原理:3FexOy+2yAl 3xFe+yAl2O3.现将铁的某种氧化物与铝粉混合、平均分成两等份.一份将足量的稀硫酸直接加入混合物,另一份先高温加热固体混合物,使之充分反应,待冷却后再加入足量的稀硫酸,二者均产生氢气且氢气的质量比为4:3.铁的氧化物中X与Y的比值为
3xFe+yAl2O3.现将铁的某种氧化物与铝粉混合、平均分成两等份.一份将足量的稀硫酸直接加入混合物,另一份先高温加热固体混合物,使之充分反应,待冷却后再加入足量的稀硫酸,二者均产生氢气且氢气的质量比为4:3.铁的氧化物中X与Y的比值为
- A.1:1
- B.1:2
- C.2:3
- D.3:4
D
分析:根据金属的强弱关系铝>铁>氢,铁与铝均能与硫酸反应生成氢气,据题意可知,反应3FexOy+2yAl 3xFe+yAl2O3中参加反应的铝与生成铁若都与足量的稀硫酸反应反放出氢气的质量比为4:3;根据反应放出氢气的质量,利用一定量金属完全反应放出氢气质量=
3xFe+yAl2O3中参加反应的铝与生成铁若都与足量的稀硫酸反应反放出氢气的质量比为4:3;根据反应放出氢气的质量,利用一定量金属完全反应放出氢气质量=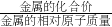 ×金属的质量,计算反应中两中金属的质量比;最后由两金属金属的质量比确定反应中x、y的值.
×金属的质量,计算反应中两中金属的质量比;最后由两金属金属的质量比确定反应中x、y的值.
解答:根据题意,反应3FexOy+2yAl 3xFe+yAl2O3中参加反应的铝与生成铁若都与足量的稀硫酸反应反放出氢气的质量比为4:3;
3xFe+yAl2O3中参加反应的铝与生成铁若都与足量的稀硫酸反应反放出氢气的质量比为4:3;
则反应中铝、铁两金属的质量比=(4÷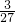 ):(3÷
):(3÷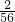 )=36:84=3:7;
)=36:84=3:7;
根据反应的化学方程式3FexOy+2yAl 3xFe+yAl2O3,反应中铝与铁的质量比=54y:168x;
3xFe+yAl2O3,反应中铝与铁的质量比=54y:168x;
则54y:168x=3:7,解得x:y=3:4
故选D.
点评:根据铁在与酸发生置换反应时表现出+2价,因此在使用一定量金属完全反应放出氢气质量=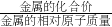 ×金属的质量时,其中铁的化合价为2.
×金属的质量时,其中铁的化合价为2.
分析:根据金属的强弱关系铝>铁>氢,铁与铝均能与硫酸反应生成氢气,据题意可知,反应3FexOy+2yAl
 3xFe+yAl2O3中参加反应的铝与生成铁若都与足量的稀硫酸反应反放出氢气的质量比为4:3;根据反应放出氢气的质量,利用一定量金属完全反应放出氢气质量=
3xFe+yAl2O3中参加反应的铝与生成铁若都与足量的稀硫酸反应反放出氢气的质量比为4:3;根据反应放出氢气的质量,利用一定量金属完全反应放出氢气质量=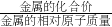 ×金属的质量,计算反应中两中金属的质量比;最后由两金属金属的质量比确定反应中x、y的值.
×金属的质量,计算反应中两中金属的质量比;最后由两金属金属的质量比确定反应中x、y的值.解答:根据题意,反应3FexOy+2yAl
 3xFe+yAl2O3中参加反应的铝与生成铁若都与足量的稀硫酸反应反放出氢气的质量比为4:3;
3xFe+yAl2O3中参加反应的铝与生成铁若都与足量的稀硫酸反应反放出氢气的质量比为4:3;则反应中铝、铁两金属的质量比=(4÷
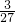 ):(3÷
):(3÷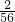 )=36:84=3:7;
)=36:84=3:7;根据反应的化学方程式3FexOy+2yAl
 3xFe+yAl2O3,反应中铝与铁的质量比=54y:168x;
3xFe+yAl2O3,反应中铝与铁的质量比=54y:168x;则54y:168x=3:7,解得x:y=3:4
故选D.
点评:根据铁在与酸发生置换反应时表现出+2价,因此在使用一定量金属完全反应放出氢气质量=
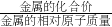 ×金属的质量时,其中铁的化合价为2.
×金属的质量时,其中铁的化合价为2. 
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
铝热反应常用于冶炼或焊接金属,反应原理:3CuO+2Al
3Cu+Al2O3.现高温加热铝粉和氧化铜混合物,使其充分反应.为检验反应后氧化铜是否有剩余,取少量反应后的固体,加入足量稀硫酸,反应后将锌片插入上层溶液中.
(已知CuO+H2SO4═CuSO4+H2O)下列现象能说明氧化铜有剩余的是( )
| ||
(已知CuO+H2SO4═CuSO4+H2O)下列现象能说明氧化铜有剩余的是( )
| A、加入稀硫酸后有气泡生成 |
| B、加入稀硫酸后没有气泡生成 |
| C、铝粉和氧化铜加热后有红色物质生成 |
| D、锌片表面有红色物质生成 |