题目内容
某氯化铵(NH4Cl)样品含氮21%,则该样品中混有的氮肥是( )
| A、CO(NH2)2 |
| B、(NH4)2SO4 |
| C、NH4NO3 |
| D、NH4HCO3 |
考点:元素的质量分数计算
专题:化学式的计算
分析:首先计算纯净物NH4Cl中氮元素的质量分数,然后与样品中氮的质量分数相比,看谁的高.若样品中的高,则杂质中氮的质量分数必定高于样品含氮量的;若样品中的低,则杂质中氮的质量分数必然低于样品含氮的质量分数.进行分析解答.
解答:解:纯净物NH4Cl中氮元素的质量分数=
×100%=26.2%,
A、CO(NH2)2中氮元素的质量分数为:
×100%=46.7%,
B、(NH4)2SO4中氮元素的质量分数为:
×100%=21.2%,
C、NH4NO3中氮元素的质量分数为:
×100%=35%,
D、NH4HCO3中氮元素的质量分数为:
×100%=17.8%,
样品中氮的质量分数为21%,由此可知样品中的低,则杂质中氮的质量分数必定低于21%;
故选D.
| 14 |
| 58.5 |
A、CO(NH2)2中氮元素的质量分数为:
| 28 |
| 60 |
B、(NH4)2SO4中氮元素的质量分数为:
| 28 |
| 132 |
C、NH4NO3中氮元素的质量分数为:
| 28 |
| 80 |
D、NH4HCO3中氮元素的质量分数为:
| 14 |
| 79 |
样品中氮的质量分数为21%,由此可知样品中的低,则杂质中氮的质量分数必定低于21%;
故选D.
点评:将质量分数的计算与生活实际相联系;计算时要理清各个量之间的关系,再结合题意进行分析解答.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
下列各组物质按酸、碱、盐的顺序排列正确的是( )
| A、MgO、H2SO4、CaCl2 |
| B、Na2SO4、Ca(OH)2、KCl |
| C、CH3COOH、KOH、K2CO3 |
| D、CH3OH、CH4、C2H5OH |
下列是某合作学习小组对物质进行的分类,正确的是( )
| A、冰、干冰既是纯净物又是化合物 |
| B、盐酸、食醋既是化合物又是酸 |
| C、不锈钢和我们日常生活中使用的硬币都是合成材料 |
| D、纯碱和熟石灰都是碱 |
某纯净物在氧气中完全燃烧,生成二氧化碳和水(无其他生成物).对该物质组成的推断正确的是( )
| A、一定含有碳,氢两种元素 |
| B、可能含有氧元素 |
| C、一定不含氧元素 |
| D、一定含碳、氢、氧三种元素 |
擦然一根火柴,火柴头向上放置,一会儿火柴就熄灭了,火柴熄灭的主要原因是( )
| A、火柴梗太潮湿 |
| B、缺乏氧气 |
| C、火柴梗不可燃 |
| D、热量散失且温度没有达到火柴梗的着火点 |
“达菲”是治疗甲型H1N1流感的一种特效药.该药物的主要成分是一种化学式为C16H31N2PO8的物质.关于该物质的说法正确的是( )
| A、达菲是由C、H、N、P、O五种元素组成 |
| B、达菲是由碳、氢、氧、氮、磷原子构成 |
| C、达菲中在碳元素和氧元素的质量之比为2:1 |
| D、达菲分子是由16个碳原子、31个氢原子、8个氧原子、2个氮原子和1个磷原子构成 |
下面是学生对课本中图表资料的使用情况,其中不正确的是( )
| A、根据金属活动性顺序表,判断金属能否与稀酸反应以及产生氢气的快慢 |
| B、根据元素周期表可判断元素在自然界的含量以及原子序数和相对原子质量 |
| C、根据金属活动性顺序表,判断金属能否与盐溶液反应以后反应的先后 |
| D、根据常见元素及原子团的化合价,判断常见化合物的化学式书写是否正确 |

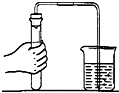 实验室在制取气体时,必须首先检查装置的气密性,如图所示.如果装置不漏气导管口就会有气泡冒出.用分子观点解释产生上述现象的原因.
实验室在制取气体时,必须首先检查装置的气密性,如图所示.如果装置不漏气导管口就会有气泡冒出.用分子观点解释产生上述现象的原因.