题目内容
神舟六号飞船载着两名宇航员圆满完成任务,胜利凯旋.宇航员们在太空还作了大量材料科学、生命科学试验及空间天文和空间环境探测等项目的研究.(1)为了使宇航员拥有一个稳定、良好的生存环境,科学家们在飞船内安装了盛有过氧化钠(Na2O2)颗粒的装置,它的用途是产生氧气.过氧化钠能吸收二氧化碳,产生碳酸钠(Na2CO3)和氧气,该反应的化学方程式 .
(2)如果1名宇航员每天需消耗860克氧气,整个宇宙飞行按6天计算,2名宇航员至少需消耗多少克Na2O2?(相对原子质量:Na-23 C-12 O-16)
【答案】分析:(1)根据题干中所提供的反应物和生成物,利用质量守恒定律配平即可.
(2)首先计算出6天宇航员所需氧气,然后利用化学方程式进行计算.
解答:解:(1)由题中信息可知Na2O2和二氧化碳反应生成了碳酸钠和氧气,配平即可.
故答案为:2Na2O2+2CO2=2Na2CO3+O2
(2)6天宇航员所需氧气的质量为:2×860×6=10320克
设需消耗x克Na2O2
2Na2O2 +2CO2 =2Na2CO3 +O2
156 32
x 10320g
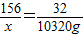
解之得:x=50310克
答:需消耗Na2O2 50310克.
点评:本题比较简单,主要考查学生配平方程式的能力和利用化学方程式进行简单计算的能力.
(2)首先计算出6天宇航员所需氧气,然后利用化学方程式进行计算.
解答:解:(1)由题中信息可知Na2O2和二氧化碳反应生成了碳酸钠和氧气,配平即可.
故答案为:2Na2O2+2CO2=2Na2CO3+O2
(2)6天宇航员所需氧气的质量为:2×860×6=10320克
设需消耗x克Na2O2
2Na2O2 +2CO2 =2Na2CO3 +O2
156 32
x 10320g
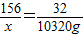
解之得:x=50310克
答:需消耗Na2O2 50310克.
点评:本题比较简单,主要考查学生配平方程式的能力和利用化学方程式进行简单计算的能力.

练习册系列答案
相关题目