题目内容
【题目】已知铁在高温条件下与氧化铜反应:2Fe+3CuO![]() Fe2O3+3Cu,铜在氯化铁溶液中发生反应:Cu+2FeCl3=2FeCl2+CuCl2。一定质量的铁与氧化铜的混合物,在高温条件下恰好完全反应。将反应后的固体粉末倒入盛有足量稀盐酸的烧杯中,振荡,充分反应后静置,然后从烧杯中取适量溶液(表示为“甲”)于试管中,并加入一定质量的锌粉,充分反应后过滤,得到滤液乙和固体丙。下列判断正确的是
Fe2O3+3Cu,铜在氯化铁溶液中发生反应:Cu+2FeCl3=2FeCl2+CuCl2。一定质量的铁与氧化铜的混合物,在高温条件下恰好完全反应。将反应后的固体粉末倒入盛有足量稀盐酸的烧杯中,振荡,充分反应后静置,然后从烧杯中取适量溶液(表示为“甲”)于试管中,并加入一定质量的锌粉,充分反应后过滤,得到滤液乙和固体丙。下列判断正确的是
①甲中不含FeCl3
②甲中含有FeCl3
③若向固体丙加稀盐酸无明显现象,则滤液乙中一定含有ZnCl2、FeCl2,可能含有CuCl2④若向固体丙加稀盐酸有气体产生,则滤液乙中可能含有ZnCl2、FeCl2,一定不含有CuCl2
A.①③ B.②③ C.①④ D.②④
【答案】A
【解析】
试题分析:铁在高温条件下与氧化铜反应:2Fe+3CuO![]() Fe2O3+3Cu, 铜在氯化铁溶液中发生反应:Cu+2FeCl3=2FeCl2+CuCl2以及Fe2O3+6HCl=2FeCl3+3H2O可以建立以下关系式:Fe2O3~2FeCl3~Cu根据铁在高温条件下与氧化铜反应:2Fe+3CuO
Fe2O3+3Cu, 铜在氯化铁溶液中发生反应:Cu+2FeCl3=2FeCl2+CuCl2以及Fe2O3+6HCl=2FeCl3+3H2O可以建立以下关系式:Fe2O3~2FeCl3~Cu根据铁在高温条件下与氧化铜反应:2Fe+3CuO![]() Fe2O3+3Cu可知生成物质氧化铁和铜的个数比是1:3,因此氯化铁一定能完全被铜反应,所以甲中不含FeCl3;所以溶液中存在FeCl2和CuCl2,由于相关金属的活动性顺序是锌>铁>铜,所以放入锌粒后锌首先置换出铜,所以固体若向固体丙加稀盐酸无明显现象,说明固体不是铁和锌,所以滤液乙中一定含有ZnCl2、FeCl2,可能含有CuCl2,若向固体丙加稀盐酸有气体产生,说明固体可能是锌或铁,因此溶液中不可能含有CuCl2,一定含有ZnCl2可能含有FeCl2,综上所述①③正确;选A。
Fe2O3+3Cu可知生成物质氧化铁和铜的个数比是1:3,因此氯化铁一定能完全被铜反应,所以甲中不含FeCl3;所以溶液中存在FeCl2和CuCl2,由于相关金属的活动性顺序是锌>铁>铜,所以放入锌粒后锌首先置换出铜,所以固体若向固体丙加稀盐酸无明显现象,说明固体不是铁和锌,所以滤液乙中一定含有ZnCl2、FeCl2,可能含有CuCl2,若向固体丙加稀盐酸有气体产生,说明固体可能是锌或铁,因此溶液中不可能含有CuCl2,一定含有ZnCl2可能含有FeCl2,综上所述①③正确;选A。

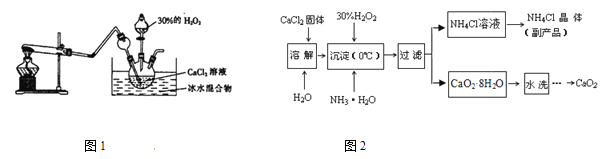
【题目】为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的速率影响效果,某研究小组进行了如下探究:

【定性研究】
(1)如图甲,可通过观察_________________来定性比较两者的速率影响效果。
【定量研究】
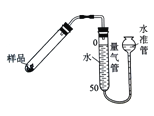
(2)如图乙,实验前检查该装置气密性的方法是__________________________。要定量比较两者的速率影响效果,可测量生成等体积气体所需的_______________。
【深入研究】
(3)在FeCl3溶液中,究竟是哪种粒子影响过氧化氢的分解速率?
猜想1:水分子(H2O)影响过氧化氢的分解速率;
猜想2:___________影响过氧化氢的分解速率;
猜想3:___________影响过氧化氢的分解速率;……
请设计实验,验证猜想
实验操作 | 实验现象 | 实验结论 |
分别取同温度同体积同浓度的H2O2溶液于2支试管中,再分别加入等质量的FeCl3和NaCl。观察现象。 | 加入FeCl3的试管中产生的气体快,加入NaCl的试管中产生的气体慢。 | 证明是Fe3+影响过氧化氢的分解速率 |
(4)【反思与讨论】上述实验确实可以证明Fe3+可以改变过氧化氢的分解速率,但不能证明FeCl3是过氧化氢分解的催化剂。若要证明FeCl3是过氧化氢分解的催化剂,还需要通过实验证明FeCl3在反应前后 ___________________ 。
请写出FeCl3催化H2O2分解的化学方程式___________________________________。