题目内容
在硝酸铜和硝酸银的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤液中滴加氯化钠溶液,有白色沉淀产生,则此时溶液中含有的溶质为 .
考点:金属的化学性质,盐的化学性质
专题:金属与金属材料
分析:根据金属活动性,判断金属与盐溶液发生反应的关系,并依据滤液中金属离子判断析出金属;根据滤液与稀盐酸反应的现象,判断过滤得到的金属的组成.
解答:解:向滤液中滴加氯化钠溶液出现白色沉淀,说明滤液中含有硝酸银溶液;
在硝酸银、硝酸铜的混合溶液中加入一定量的铁粉,根据金属活动性,铁粉首先与硝酸银反应,硝酸银被完全置换后,铁粉开始与硝酸铜进行置换反应;而铜与硝酸银也能反应生成银,溶液中有硝酸银,则固体不可能存在铜;由于滤液中含有硝酸银,说明加入的铁粉不足,没能完全置换出溶液中的银离子,所以,析出的金属只有银.而此时溶液中含有的溶质为硝酸银、硝酸铜、硝酸亚铁.
故答案为:
硝酸银、硝酸铜、硝酸亚铁
在硝酸银、硝酸铜的混合溶液中加入一定量的铁粉,根据金属活动性,铁粉首先与硝酸银反应,硝酸银被完全置换后,铁粉开始与硝酸铜进行置换反应;而铜与硝酸银也能反应生成银,溶液中有硝酸银,则固体不可能存在铜;由于滤液中含有硝酸银,说明加入的铁粉不足,没能完全置换出溶液中的银离子,所以,析出的金属只有银.而此时溶液中含有的溶质为硝酸银、硝酸铜、硝酸亚铁.
故答案为:
硝酸银、硝酸铜、硝酸亚铁
点评:金属与盐的混合溶液反应时,置换反应按金属活动性由弱到强的顺序先后反应,首先把溶液中金属活动性最弱的金属从溶液中置换出来.

练习册系列答案
相关题目
下列物质间的转化,不能通过一步反应实现的是( )
| A、CO2→CaCO3 |
| B、CO→CO2 |
| C、H2O2→O2 |
| D、Cu→Cu(OH)2 |
下列常见物质在生活中使用不当的是( )
| A、做馒头时用纯碱中和发酵中产生的酸 |
| B、铁锈通常用稀盐酸洗去 |
| C、酸雨侵蚀后的土壤通常播撒熟石灰 |
| D、治疗胃酸过多的药物中通常含有氢氧化钠 |
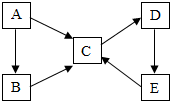 A、B、C、D、E均为初中化学常见的物质,它们之间的转化关系如图所示(其中“→”表示某一种物质经一步反应可转化为另一种物质,部分反应物、生成物和反应条件已略去).
A、B、C、D、E均为初中化学常见的物质,它们之间的转化关系如图所示(其中“→”表示某一种物质经一步反应可转化为另一种物质,部分反应物、生成物和反应条件已略去).