题目内容
废旧干电池中许多物质是可以回收利用的,某学校研究小组对废干电池内的填充物(含有C、MnO2、ZnCl2、NH4Cl)进行探究,实验过程如下:

(1)操作②的名称是 ,操作③中玻璃棒的作用是 .
(2)操作④的试管中产生的气体能使带火星的木条复燃,产生该气体的化学方程式是: .
(3)ZnCl2和NH4Cl混合溶液中含有杂质CuCl2,会加速对电池的腐蚀,欲除去Cu2+,最好选用下列试剂中的 (填字母序号).
A、NaOH B、Zn C、Fe D、Na2CO3
部分物质的溶解性表

(1)操作②的名称是
(2)操作④的试管中产生的气体能使带火星的木条复燃,产生该气体的化学方程式是:
(3)ZnCl2和NH4Cl混合溶液中含有杂质CuCl2,会加速对电池的腐蚀,欲除去Cu2+,最好选用下列试剂中的
A、NaOH B、Zn C、Fe D、Na2CO3
部分物质的溶解性表
| OH+ | Cl- | CO3 2- | |||
NH
| 溶、挥 | 溶 | 溶 | ||
| Na+ | 溶 | 溶 | 溶 | ||
| Zn2+ | 不 | 溶 | 不 | ||
| Cu2+ | 不 | 溶 | 不 |
考点:实验探究物质的组成成分以及含量,过滤的原理、方法及其应用,实验室制取氧气的反应原理,金属的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)根据玻璃棒在如图操作中的作用进行分析;
(2)根据过氧化氢在二氧化锰的催化作用下会生成水和氧气进行分析;
(3)根据除去杂质的原则可知,既要除去杂质离子又要不能引入新的杂质离子进行分析.
(2)根据过氧化氢在二氧化锰的催化作用下会生成水和氧气进行分析;
(3)根据除去杂质的原则可知,既要除去杂质离子又要不能引入新的杂质离子进行分析.
解答:解:(1)通过分析图中的操作可知,操作②是过滤,操作③是蒸发,玻璃棒的作用是:使液体均匀受热,防止局部过热,造成液滴飞溅;
(2)过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2
2H2O+O2↑;
(3)ZnCl2和NH4Cl混合溶液中含有杂质CuCl2,实际上就是除去Cu2+即可,若选用NaOH会和三种物质都反应,若选用Fe会引入新杂质离子亚铁离子,若选用Na2CO3会使原物质发生反应的同时引入杂质离子钠离子,只有固体Zn即能除去杂质离子Cu2+又不引入新的杂质离子,故选:B.
故答案为:(1)过滤,使液体均匀受热,防止局部过热,造成液滴飞溅;
(2)2H2O2
2H2O+O2↑;
(3)B.
(2)过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2
| ||
(3)ZnCl2和NH4Cl混合溶液中含有杂质CuCl2,实际上就是除去Cu2+即可,若选用NaOH会和三种物质都反应,若选用Fe会引入新杂质离子亚铁离子,若选用Na2CO3会使原物质发生反应的同时引入杂质离子钠离子,只有固体Zn即能除去杂质离子Cu2+又不引入新的杂质离子,故选:B.
故答案为:(1)过滤,使液体均匀受热,防止局部过热,造成液滴飞溅;
(2)2H2O2
| ||
(3)B.
点评:本题以电池为情景素材,考查了干电池物质成分的探究、常见的分化学实验基本操作及灵活运用所学知识进行解决问题的能力.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
下列离子反应方程式,书写正确的是( )
| A、碳酸钠溶液中加入盐酸 CO32-+2H+═H2O+CO2↑ |
| B、稀硫酸中加入铁粉 2Fe+6H+═2Fe3++3H2↑ |
| C、碳酸钙中加入盐酸 CO32-+2H+═H2O+CO2↑ |
| D、氢氧化钡溶液中加入硫酸 H++OH-═H2O |
下列物质都属于混合物的是( )
| A、海水、水银 |
| B、石墨、氧化铁 |
| C、干冰、冰水混合物 |
| D、不锈钢菜刀、铁矿石 |
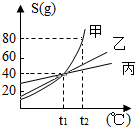 如图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息错误的是( )
如图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息错误的是( )| A、t2℃时丙物质的溶解度最小 |
| B、甲物质的溶解度受温度的影响最大 |
| C、要使t1℃时甲物质的饱和溶液变成不饱和溶液,可以采取升高温度的方法 |
| D、t2℃时,往100g水中加入90g乙物质,充分搅拌后得到190g乙物质的溶液 |
类推是学习化学的一种重要方法,以下类推正确的是( )
| A、碱能跟非金属氧化物反应,则碱溶液一定能吸收CO2、SO2和CO |
| B、物质都由元素组成,同种元素可组成纯净物,则不同种元素也可组成纯净物 |
| C、分解反应能生成两种或两种以上其他物质,则生成两种或两种以上其他物质的反应一定是分解反应 |
| D、钠原子核外最外电子层上排布着一个电子,属于金属元素的原子,则最外电子层上排布着一个电子的原子一定是金属元素的原子 |

 A~H是初中化学常见的物质,A和C的组成元素相同、在常温下均为液体,B为单质,D为石灰水的主要成分,E为一种常见的建筑材料.它们的相互转化关系如图所示(反应条件、部分生成物已略去).
A~H是初中化学常见的物质,A和C的组成元素相同、在常温下均为液体,B为单质,D为石灰水的主要成分,E为一种常见的建筑材料.它们的相互转化关系如图所示(反应条件、部分生成物已略去).