题目内容
【题目】在“宏观—微观—符号”之间建立联系,是学习化学的一种重要思维方式。下图是元素周期表中部分元素的原子结构示意图,根据所学知识回答下列问题。
A. 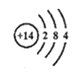 B.
B. 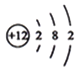 C.
C. 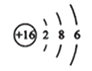 D.
D.  E.
E.  F.
F. 
(1)上图A、B、C、D元素中,属于金属元素的是 (填元素符号);
(2)D原子在化学反应中易(填“得到”或“失去”)电子;
(3)由B元素和D元素组成的化合物的化学式为;
(4)E粒子带1个单位正电荷,则X=,离子的符号为;
(5)F为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是。
a.原子序数Z>Y b.核外电子数:X=Y c.Y和Z处于同一族
【答案】
(1)Mg
(2)得到
(3)MgCl2
(4)11;Na+
(5)a
【解析】(1)由质子数可知A-14-Si-硅,B-12-Mg-镁,C-16-S-硫,D-17-Cl-氯,因此金属元素为Mg;(2)D最外层电子数为7>4,易得到1个电子形成8电子的稳定结构;(3)Mg显+2价,Cl显-1价,化合物中元素化合价代数和为0,因此化学式为MgCl2 ;(4)E粒子带1个单位正电荷,即失去了一个电子,那么原子时其电子数=10+1=11=质子数=X,为钠元素;为带1个正电荷的钠离子;(5)由元素周期律规则可知,a、ZY同一周期,原子序数从左到右依次递增,因此原子序数Z>Y,正确;b、X、Y同族,最外层电子数相等,不是电子数,因此错误;c、Y、Z处于同周期,不是同族,错误。

练习册系列答案
相关题目