题目内容
14世纪,欧洲旅行家马可?波罗在他的《东方见闻记》中曾描述:“中国人的燃料是一种黑石头…”他所说的燃烧的“黑石头”就是煤.其实,在他见到中国人用煤以前,中国人已经用煤一千多年了.煤是一种重要的化工原料,用煤作燃料,不仅是极大的浪费,而且因烟煤中含有硫的化合物(如FeS2),燃烧会产生SO2而污染环境.
若煤中含FeS25%,假设燃烧时硫全部转化为SO2而排入大气中,其燃烧化学方程式如下:
4FeS2+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
(1)我国计划从2001年至2005年,将SO2排放量从每年1995万吨降至1800万吨,意味着2005年比2001年可少燃烧这种煤多少万吨?
(2)为了消除SO2对空气的污染,可用烧碱溶液吸收.那么2005年比2001年可以节约烧碱固体多少万吨?
(1)解:设2005年比2001年可少燃烧这种煤的质量为x
二氧化硫减少的质量是:1995万吨-1800万吨=195万吨
4FeS2+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
480 512
5%x 195万吨
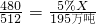
则x=3656.25万吨.
答:2005年比2001年可少燃烧这种煤的质量为3656.25万吨.
(2)解:设2005年比2001年可节约烧碱固体的质量为y.
2NaOH+SO2=Na2SO3+H2O
80 64
y 195万吨
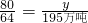
y=243.75万吨.
答:2005年比2001年可节约烧碱固体的质量为243.75万吨.
分析:可以根据化学方程式方面的知识进行分析、计算,从而得出正确的结论.根据4FeS2+11O2 2Fe2O3+8SO2及其相关方面的数据可以求出某些物质的质量.
2Fe2O3+8SO2及其相关方面的数据可以求出某些物质的质量.
点评:解答本题的关键是要掌握根据化学方程式计算的方法,准确分析数据所对应的量才能对计算方面的问题做出正确的判断.
二氧化硫减少的质量是:1995万吨-1800万吨=195万吨
4FeS2+11O2
 2Fe2O3+8SO2
2Fe2O3+8SO2480 512
5%x 195万吨
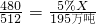
则x=3656.25万吨.
答:2005年比2001年可少燃烧这种煤的质量为3656.25万吨.
(2)解:设2005年比2001年可节约烧碱固体的质量为y.
2NaOH+SO2=Na2SO3+H2O
80 64
y 195万吨
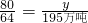
y=243.75万吨.
答:2005年比2001年可节约烧碱固体的质量为243.75万吨.
分析:可以根据化学方程式方面的知识进行分析、计算,从而得出正确的结论.根据4FeS2+11O2
 2Fe2O3+8SO2及其相关方面的数据可以求出某些物质的质量.
2Fe2O3+8SO2及其相关方面的数据可以求出某些物质的质量.点评:解答本题的关键是要掌握根据化学方程式计算的方法,准确分析数据所对应的量才能对计算方面的问题做出正确的判断.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 2Fe2O3+8SO2
2Fe2O3+8SO2