题目内容
(2011?柳州)某课外活动小组为研究由锌和铜组成的黄铜样品中各成分含量,做了以下实验.取黄铜样品粉末20g于烧杯中,将100g19.6%的稀硫酸分2次加入烧杯中(假设每次均充分反应),得到以下数据:
已知:锌与稀硫酸反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑,计算:
(1)生成气体的总质量为
(2)样品中铜(Cu)的质量为多少?(请写出计算过程)
(3)完全反应后所得溶液总质量为
| 加入稀硫酸的次数 | 第1次 | 第2次 |
| 加入稀硫酸质量/g | 50 | 50 |
| 生成气体的质量/g | 0.20 | 0.10 |
(1)生成气体的总质量为
0.3
0.3
g.(2)样品中铜(Cu)的质量为多少?(请写出计算过程)
(3)完全反应后所得溶液总质量为
109.45g
109.45g
.分析:根据金属活动顺序表可知铜和锌的合金中只有锌能与稀硫酸反应生成氢气;由表格数据可知第二次加50g稀硫酸时,锌已经反应完全,总共收集到氢气为两次之和;再根据化学方程式,利用氢气的质量求出锌的质量,然后再求出合金中铜的质量分数,同时也可以依据质量守恒定律求出反应后溶液的总质量;
解答:解:(1)比较第2次和第1次产生的氢气的质量可以知道,第2次锌就已反应完全,所以根据表格中数据可以计算出产生的氢气的质量为:0.2g+0.1g=0.3g.
(2)设黄铜中锌的质量为x,生成氯化锌的质量为y.
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.30g
=
x=9.75g
所以样品中铜的质量是20g-9.75g=10.25g
(3)反应后的溶液质量是9.75g+100g-0.30g=109.45
故答案为:(1)0.3;(2)样品中铜(Cu)的质量为10.25g;(3)109.45g;
(2)设黄铜中锌的质量为x,生成氯化锌的质量为y.
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.30g
| 65 |
| x |
| 2 |
| 0.30g |
x=9.75g
所以样品中铜的质量是20g-9.75g=10.25g
(3)反应后的溶液质量是9.75g+100g-0.30g=109.45
故答案为:(1)0.3;(2)样品中铜(Cu)的质量为10.25g;(3)109.45g;
点评:要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
相关题目
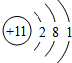 (2011?柳州)如图是某元素的原子结构示意图,该原子的质子数为
(2011?柳州)如图是某元素的原子结构示意图,该原子的质子数为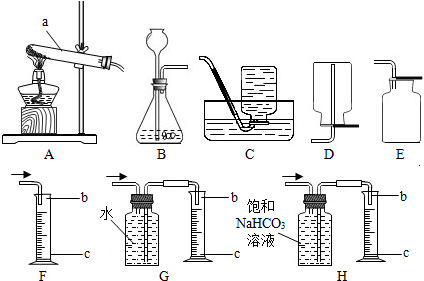
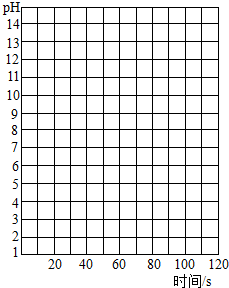
 (2011?柳州)某化学兴趣小组的同学按照课本的实验装置做“测定空气中氧气的体积分数”实验(图1),但测出的氧气体积分数明显小于
(2011?柳州)某化学兴趣小组的同学按照课本的实验装置做“测定空气中氧气的体积分数”实验(图1),但测出的氧气体积分数明显小于