题目内容
 在化学反应前后,物质的总质量会发生变化吗?针对此问题,
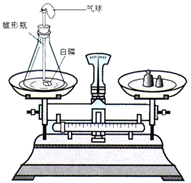
在化学反应前后,物质的总质量会发生变化吗?针对此问题,小王同学通过下面的实验进行探究.
【猜想假设】猜想1:化学反应前后物质的总质量增大;猜想2:化学反应
前后物质的总质量
减小
减小
;猜想3:化学反应前后物质的总质量不变
不变
.【设计实验】到底哪种猜想正确?小王想设计了下面的实验进行探究.
实验:用热的玻璃棒点燃白磷,使其燃烧,测定反应前后物质的质量变化.
【实验现象】白磷燃烧产生
大量白烟
大量白烟
;气球先变大,后又变小.天平最后仍平衡.
【实验反思】(1)实验中气球先变大,后又变小的原因是
白磷燃烧放热,气球膨胀
白磷燃烧放热,气球膨胀
燃烧消耗氧气并冷却到室温,瓶内气压减小,气球变小
燃烧消耗氧气并冷却到室温,瓶内气压减小,气球变小
.小王根据该实验现象,再结合前面所学的碳酸钙和盐酸反应前后的质量变化情况的实验探究得出了下列结论:当用有气体参加或生成的化学反应来验证质量守恒定律时,应在
密闭容器内
密闭容器内
,才能判定参加化学反应的反应物总质量和生成物总质量是否相等.分析:[猜想假设]根据题中信息可知化学反应前后物质的总质量的变化情况有增大、减小、不变;
[实验现象]根据白磷燃烧的现象分析;
[实验反思]白磷燃烧放热,气球膨胀,燃烧消耗氧气并冷却到室温,瓶内气压减小,气球变小;来验证质量守恒定律时,应在密闭容器内进行.
[实验现象]根据白磷燃烧的现象分析;
[实验反思]白磷燃烧放热,气球膨胀,燃烧消耗氧气并冷却到室温,瓶内气压减小,气球变小;来验证质量守恒定律时,应在密闭容器内进行.
解答:解:[猜想假设]根据题中信息可知化学反应前后物质的总质量的变化情况有增大、减小、不变;
故答案为:减小;不变;
[实验现象]白磷燃烧产生大量的白烟,故答案为:大量白烟;
[实验反思]白磷燃烧放热,气球膨胀,燃烧消耗氧气并冷却到室温,瓶内气压减小,气球变小;当用有气体参加或生成的化学反应来验证质量守恒定律时,应在密闭容器中才能判定参加化学反应的反应物总质量和生成物总质量是否相等.故答案为:白磷燃烧放热,气球膨胀;燃烧消耗氧气并冷却到室温,瓶内气压减小,气球变小;密闭容器内.
故答案为:减小;不变;
[实验现象]白磷燃烧产生大量的白烟,故答案为:大量白烟;
[实验反思]白磷燃烧放热,气球膨胀,燃烧消耗氧气并冷却到室温,瓶内气压减小,气球变小;当用有气体参加或生成的化学反应来验证质量守恒定律时,应在密闭容器中才能判定参加化学反应的反应物总质量和生成物总质量是否相等.故答案为:白磷燃烧放热,气球膨胀;燃烧消耗氧气并冷却到室温,瓶内气压减小,气球变小;密闭容器内.
点评:本题主要考察了对质量守恒定律的探究,通过该题培养了学生的分析问题的能力,难度不大.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
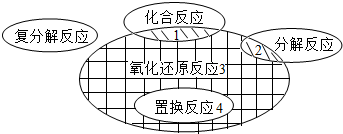 在化学反应前后,物质所含元素化合价发生变化的反应是氧化还原反应,它与化学反应基本类型间的关系如图所示,下列示例中错误的是( )
在化学反应前后,物质所含元素化合价发生变化的反应是氧化还原反应,它与化学反应基本类型间的关系如图所示,下列示例中错误的是( )A、阴影1:C+O2
| ||||
B、阴影2:2H2O
| ||||
| C、阴影3:Mg(OH)2+2HCl=MgCl2+2H2O | ||||
| D、阴影4:Fe+CuSO4=FeSO4+Cu |

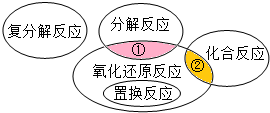 在化学反应前后,物质所含元素化合价发生变化的反应是氧化还原反应,它与九年级所学的化学基本反应类型间的关系如图所示.请各写出一例属于阴影①、②处的化学反应方程式
在化学反应前后,物质所含元素化合价发生变化的反应是氧化还原反应,它与九年级所学的化学基本反应类型间的关系如图所示.请各写出一例属于阴影①、②处的化学反应方程式
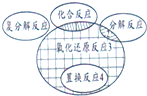 在化学反应前后,物质所含元素化合价发生变化的反应是氧化还原反应,它与化学反应基本类型间的关系如图所示,下列示例中正确的是( )
在化学反应前后,物质所含元素化合价发生变化的反应是氧化还原反应,它与化学反应基本类型间的关系如图所示,下列示例中正确的是( )