题目内容
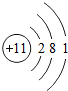
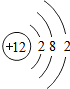
核电荷数为1~18的元素的原子结构示意图如图,回答下列问题:
(1)表中不同元素最本质的区别是 .
(2)在第三周期中,各原子结构的共同之处是 ,该周期中,各原子核外电子排布地变化规律是 .
(3)在第三周期中,元素类型的变化情况是:从左到右由 元素过渡到 元素,并以稀有气体元素结尾.
(4)核电荷数为12的元素失去两个电子后,形成的粒子的符号是 ,它的核外电子排布与
元素的原子核外电子排布相同.
(1)表中不同元素最本质的区别是
(2)在第三周期中,各原子结构的共同之处是
(3)在第三周期中,元素类型的变化情况是:从左到右由
(4)核电荷数为12的元素失去两个电子后,形成的粒子的符号是
元素的原子核外电子排布相同.
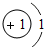 |
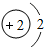 | ||||||
| 氢(H) | 氦(He) | ||||||
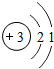 |
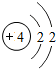 |
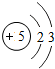 |
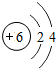 |
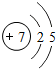 |
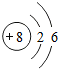 |
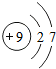 |
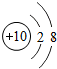 |
| 锂( Li) | 铍(Be) | 硼(B) | 碳(C) | 氮(N) | 氧(O) | 氟(F) | 氖(Ne) |
 |
 |
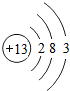 |
 |
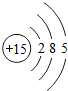 |
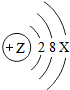 |
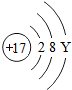 |
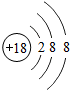 |
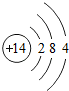
| 钠(Na) | 镁(Mg) | 铝(Al) | 硅(Si) | 磷(P) | 硫(S) | 氯(Cl) | 氩(Ar) |
分析:(1)根据元素的定义分析
(2)根据元素周期表第三周期中各原子核外电子排布分析
(3)根据每一周期元素种类分析
(4)根据原子结构示意图的特点及离子符号的书写分析
(2)根据元素周期表第三周期中各原子核外电子排布分析
(3)根据每一周期元素种类分析
(4)根据原子结构示意图的特点及离子符号的书写分析
解答:解:(1)元素是具有相同核电荷数即质子数的一类原子的总称,故不同元素最本质的区别是质子数(核电荷数)不同.
(2)在第三周期中各元素原子的电子层数相同,都是三层,该周期中,各原子核外最外层电子数由1~8依次递增.
(3)在第三周期中,从左到右元素由金属元素过渡到非金属元素,并以稀有气体元素结尾.
(4)核电荷数为12的元素为镁元素,失去两个电子后形成带两个单位正电荷的镁离子,粒子的符号是 Mg2+,它的核外电子排布与氖元素的原子核外电子排布相同.
故答案为:(1)质子数(核电荷数)不同.
(2)电子层数相同,最外层电子数由1~8依次递增.
(3)金属 非金属.
(4)Mg2+,氖
(2)在第三周期中各元素原子的电子层数相同,都是三层,该周期中,各原子核外最外层电子数由1~8依次递增.
(3)在第三周期中,从左到右元素由金属元素过渡到非金属元素,并以稀有气体元素结尾.
(4)核电荷数为12的元素为镁元素,失去两个电子后形成带两个单位正电荷的镁离子,粒子的符号是 Mg2+,它的核外电子排布与氖元素的原子核外电子排布相同.
故答案为:(1)质子数(核电荷数)不同.
(2)电子层数相同,最外层电子数由1~8依次递增.
(3)金属 非金属.
(4)Mg2+,氖
点评:本题难度不大,是常考的题型,掌握同一周期的各原子结构示意图的特点、离子符号的书写以及元素周期表的特点等是正确解答此类题的关键

练习册系列答案
相关题目
核电荷数为1~18的元素中,某微粒结构示意图为: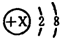 则该微粒( )
则该微粒( )
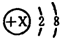 则该微粒( )
则该微粒( )| A、一定是阳离子 | B、一定是阴离子 | C、一定是氖原子 | D、无法确定 |

 ,则该离子带
,则该离子带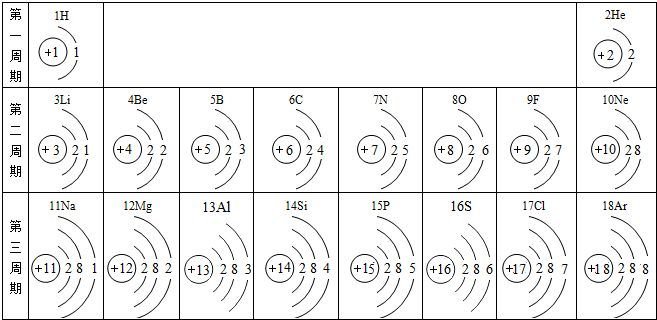 (1)在第二周期中,各原子结构的共同之处是
(1)在第二周期中,各原子结构的共同之处是