题目内容
 26、一天,实验助手小娟走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如右图).
26、一天,实验助手小娟走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如右图).(1)此情此景你首先想到的是它可能变质了,该变质反应的化学方程式为:
2NaOH+CO2═Na2CO3+H2O
.(2)围绕此瓶NaOH溶液是否变质的问题,小娟利用实验室的三种试剂(氯化钙溶液、稀盐酸、酚酞试液)展开了探究活动.
①取少量溶液于试管中,滴加某种试剂,有气泡产生,由此证明NaOH溶液已经变质.你认为小娟所加的试剂是
稀盐酸
.②也有同学认为:只要从瓶中取出少量溶液,向其中滴加酚酞试液,溶液变成红色,就可能确定能使溶液呈碱性的就是NaOH,你认为这种看法是否正确
不正确
理由是碳酸钠溶液也显碱性
③欲证明变质的溶液中尚存NaOH,请你帮助小娟完成以下探究方案:

(3)通过上述探究,说明氢氧化钠溶液暴露在空气中容易变质,故应
密封
保存.分析:(1)NaOH溶液吸收空气中的二氧化碳生成Na2CO3;;;;
(2)①2HCl+Na2CO3=2NaCl+CO2↑+H2O
②氢氧化钠可使酚酞试液变红,碳酸钠是强碱弱酸盐具有一定的碱性也会使酚酞试液显红色
③Na2CO3+CaCl2=CaCO3↓+2NaCl,酚酞遇碱变红色,如果溶液中尚存NaOH,那么在少量NaOH溶液中加入足量CaCl2溶液后再加酚酞试液则既产生白色沉淀又变红色,如果溶液中不存在NaOH,加入足量CaCl2溶液后就除尽了CO32-既没有了氢氧化钠也没有了碳酸钠只产生白色沉淀再加酚酞试液不变色.
(3)NaOH溶液易吸收空气中的二氧化碳生成Na2CO3 所以应于空气隔绝.
(2)①2HCl+Na2CO3=2NaCl+CO2↑+H2O
②氢氧化钠可使酚酞试液变红,碳酸钠是强碱弱酸盐具有一定的碱性也会使酚酞试液显红色
③Na2CO3+CaCl2=CaCO3↓+2NaCl,酚酞遇碱变红色,如果溶液中尚存NaOH,那么在少量NaOH溶液中加入足量CaCl2溶液后再加酚酞试液则既产生白色沉淀又变红色,如果溶液中不存在NaOH,加入足量CaCl2溶液后就除尽了CO32-既没有了氢氧化钠也没有了碳酸钠只产生白色沉淀再加酚酞试液不变色.
(3)NaOH溶液易吸收空气中的二氧化碳生成Na2CO3 所以应于空气隔绝.
解答:解:(1)NaOH溶液易吸收空气中的二氧化碳生成Na2CO3
故该变质反应的方程式为:2NaOH+CO2═Na2CO3+H2O
(2)①盐酸可与碳酸钠反应生成二氧化碳气体,2HCl+Na2CO3=2NaCl+CO2↑+H2O,故答案为:盐酸
②氢氧化钠可使酚酞试液变红,碳酸钠是强碱弱酸盐具有一定的碱性也会使酚酞试液显红色,故答案为:不正确;碳酸钠溶液也显碱性
③Na2CO3+CaCl2=CaCO3↓+2NaCl,酚酞遇碱变红色,如果溶液中尚存NaOH,那么在少量NaOH溶液中加入足量CaCl2溶液后再加酚酞试液则既产生白色沉淀又变红色,如果溶液中不存在NaOH,加入足量CaCl2溶液后就除尽了CO32-既没有了氢氧化钠也没有了碳酸钠再加酚酞试液只产生白色沉淀而不变色.
故答案为:
(3)NaOH溶液易吸收空气中的二氧化碳生成Na2CO3 而变质,故答案为:密封
故该变质反应的方程式为:2NaOH+CO2═Na2CO3+H2O
(2)①盐酸可与碳酸钠反应生成二氧化碳气体,2HCl+Na2CO3=2NaCl+CO2↑+H2O,故答案为:盐酸
②氢氧化钠可使酚酞试液变红,碳酸钠是强碱弱酸盐具有一定的碱性也会使酚酞试液显红色,故答案为:不正确;碳酸钠溶液也显碱性
③Na2CO3+CaCl2=CaCO3↓+2NaCl,酚酞遇碱变红色,如果溶液中尚存NaOH,那么在少量NaOH溶液中加入足量CaCl2溶液后再加酚酞试液则既产生白色沉淀又变红色,如果溶液中不存在NaOH,加入足量CaCl2溶液后就除尽了CO32-既没有了氢氧化钠也没有了碳酸钠再加酚酞试液只产生白色沉淀而不变色.
故答案为:
| 除尽溶液中的CO32- | 氯化钙溶液 | 产生白色沉淀; |
| 溶液变红 |
点评:本题通过实验探究氢氧化钠溶液是否变质是否完全变质来考查“2NaOH+CO2=Na2CO3+H2O、Na2CO3+CaCl2=CaCO3↓+2NaCl、2HCl+Na2CO3=2NaCl+CO2↑+H2O 酚酞遇碱变红色”等知识点重点培养学生通过实验现象归纳出结论的能力.

练习册系列答案
 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
 24、一天,实验助手小娟和小丽走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).
24、一天,实验助手小娟和小丽走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).
 13、一天,实验助手小娟和小丽走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).
13、一天,实验助手小娟和小丽走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).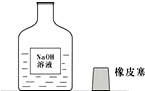 一天,实验助手小娟走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”,如图:
一天,实验助手小娟走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”,如图: