题目内容
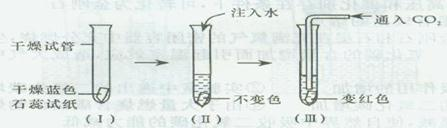
实验室常用石蕊试纸检验物质的酸碱性;已知:酸性物质使蓝色的石蕊试纸变红,碱性物质使红色的石蕊试纸变蓝.某学生想要通过碳酸氢铵分解产生的氨气来探究氨水具有碱性,而氨气不具有碱性,按图所示进行实验:

[已知NH4HCO3
NH3↑+H2O+CO2↑、2NH3+H2SO4=(NH4)2 SO4]
请按要求回答下列问题:
①向A烧杯中加浓硫酸的作用是
②若氨气不具有碱性,则C瓶中石蕊试纸(填:变蓝色、不变色 下同)
③E烧杯中稀硫酸的作用是

[已知NH4HCO3
| ||
请按要求回答下列问题:
①向A烧杯中加浓硫酸的作用是
放热使NH4HCO3分解
放热使NH4HCO3分解
,B管的作用是除去CO2和H2O
除去CO2和H2O
.②若氨气不具有碱性,则C瓶中石蕊试纸(填:变蓝色、不变色 下同)
不变色
不变色
,氨水具有碱性,则D瓶中石蕊试纸变蓝色
变蓝色
.③E烧杯中稀硫酸的作用是
吸收氨气,防止氨气污染空气
吸收氨气,防止氨气污染空气
.分析:浓硫酸溶于水放热,因此向A烧杯中加浓硫酸的作用是放热使NH4HCO3分解;氢氧化钠固体既吸收水蒸气,又吸收二氧化碳;干燥的氨气不具有碱性,石蕊试纸不变色;氨气溶于水生成氨水,D瓶中石蕊试纸变蓝色;E烧杯中稀硫酸的作用是:吸收氨气,防止氨气污染空气.
解答:解:①浓硫酸溶于水放热,因此向A烧杯中加浓硫酸的作用是放热使NH4HCO3分解;氢氧化钠固体既吸收水蒸气,又吸收二氧化碳;故答案为:放热使NH4HCO3分解; 除去CO2和H2O;
②干燥的氨气不具有碱性,石蕊试纸不变色;氨气溶于水生成氨水,D瓶中石蕊试纸变蓝色;故答案为:不变色;变蓝色;
③E烧杯中稀硫酸的作用是:吸收氨气,防止氨气污染空气.故答案为:吸收氨气,防止氨气污染空气
②干燥的氨气不具有碱性,石蕊试纸不变色;氨气溶于水生成氨水,D瓶中石蕊试纸变蓝色;故答案为:不变色;变蓝色;
③E烧杯中稀硫酸的作用是:吸收氨气,防止氨气污染空气.故答案为:吸收氨气,防止氨气污染空气
点评:本题以实验为主考查氨气的化学性质,是经常考查的典型实验.有关实验方案的设计和对实验方案的评价是中考的热点之一,设计实验方案时,要注意用最少的药品和最简单的方法;关于对实验设计方案的评价,要在两个方面考虑,一是方案是否可行,能否达到实验目的;二是设计的方法进行比较,那种方法更简便.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目