题目内容
下列说法正确的是
- A.0.5molO2约含1mol氧元素
- B.CO2的摩尔质量是44g
- C.1molH2O中含有1molH2和1molO
- D.22克CO2中共含1.5mol原子
D
分析:根据单质的概念和元素的相对原子质量解答本题.根据原子个数等于右下角数字之和;根据相对分子质量的计算公式进行计算.
解答:A、是含有1摩尔氧原子,而非氧元素,故A错误;
B、CO2的摩尔质量是44克每摩尔,故B错误;
C、1molH2O中含有2摩尔H原子和一摩尔氧原子,而非1molH2和1molO,故C错误
D、先求出二氧化碳物质的量为0.5mol,再乘以三(因为一个二氧化碳分子中含有三个原子,就是1.5mol原子),故D正确.
故选D.
点评:本题主要考查学生运用化学式进行计算的能力.一个分子中所含的原子个数等于各元素右下角的数字之和;相对分子质量等于各个原子的相对原子质量总和.
分析:根据单质的概念和元素的相对原子质量解答本题.根据原子个数等于右下角数字之和;根据相对分子质量的计算公式进行计算.
解答:A、是含有1摩尔氧原子,而非氧元素,故A错误;
B、CO2的摩尔质量是44克每摩尔,故B错误;
C、1molH2O中含有2摩尔H原子和一摩尔氧原子,而非1molH2和1molO,故C错误
D、先求出二氧化碳物质的量为0.5mol,再乘以三(因为一个二氧化碳分子中含有三个原子,就是1.5mol原子),故D正确.
故选D.
点评:本题主要考查学生运用化学式进行计算的能力.一个分子中所含的原子个数等于各元素右下角的数字之和;相对分子质量等于各个原子的相对原子质量总和.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
 26、2009年4月22日是“世界水日”.水与人类的生活和生产密切相关.请回答以下问题:
26、2009年4月22日是“世界水日”.水与人类的生活和生产密切相关.请回答以下问题: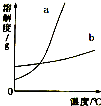 KNO3和KCl在不同温度时的溶解度如下表所示.请回答下列问题:
KNO3和KCl在不同温度时的溶解度如下表所示.请回答下列问题: