题目内容
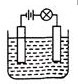
在做溶液的导电性试验时,小明向稀Ba(OH)2溶液中慢慢加入少量无水硫酸铜粉末,如图所示,小灯泡的亮度将如何变化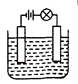
- A.不变→变亮
- B.变暗→变亮
- C.变暗
- D.不变
C
分析:根据溶液的导电性与溶液中离子多少有关进行解答.
解答:Ba(OH)2溶液中,电离出自由移动的钡离子和氢氧根离子,闭合电键时灯泡发亮;当向烧杯逐渐加入硫酸铜溶液时,硫酸铜与氢氧化钡反应生成不溶于水的硫酸钡和不溶于水的氢氧化铜,CuSO4+Ba(OH)2=BaSO4↓+Cu(OH)2↓,溶液中自由移动的离子越来越少,故灯泡越来越暗.
故选C.
点评:此题主要考查溶液导电的原因,并根据物质溶解性,判断溶液中是否存在自由移动的离子,从而确定灯泡是否发光,最终找出符合试题意图的答案.
分析:根据溶液的导电性与溶液中离子多少有关进行解答.
解答:Ba(OH)2溶液中,电离出自由移动的钡离子和氢氧根离子,闭合电键时灯泡发亮;当向烧杯逐渐加入硫酸铜溶液时,硫酸铜与氢氧化钡反应生成不溶于水的硫酸钡和不溶于水的氢氧化铜,CuSO4+Ba(OH)2=BaSO4↓+Cu(OH)2↓,溶液中自由移动的离子越来越少,故灯泡越来越暗.
故选C.
点评:此题主要考查溶液导电的原因,并根据物质溶解性,判断溶液中是否存在自由移动的离子,从而确定灯泡是否发光,最终找出符合试题意图的答案.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目