题目内容
某兴趣小组同学在一份资料中了解到:铜有CuO和Cu2O(红色)两种常见的氧化物.因为Cu和Cu2O均为红色,故他们猜测,在H2还原CuO所得的红色产物中可能含有Cu2O.(1)该小组同学准确称取了8.0g黑色CuO粉末放入大试管中,不断通入足量的H2,在加热条件下进行还原,如果产物只有Cu,其质量应为______.
(2)该小组在H2还原CuO时,当发现8.0g黑色CuO粉末全部转变成红色时,停止加热,冷却后称得固体质量为6.8g.此红色固体中氧元素的质量为______,以此推得Cu2O的质量为______.
(3)将(2)中所得的6.8g固体放入烧杯中,加入48.0g过量稀盐酸(Cu2O与稀盐酸的反应为:Cu2O+2HCl=CuCl2+Cu+H2O),充分搅拌,除有红色固体外,还发现溶液变蓝.试计算此蓝色溶液中CuCl2的质量分数.
【答案】分析:氢气的化学性质有:可燃性和还原性.根据元素守恒,可以用氧化铜的质量求铜的质量.冷却后称得固体质量为6.8g,因此有氧化亚铜,与6.4g的差值就是氧元素的质量,从而得到氧化亚铜的质量.铜与氧化亚铜的混合物,加入过量稀盐酸,只有氧化亚铜反应,铜不反应,因此根据化学方程式可以求氯化亚铜的质量,根据质量守恒定律求溶液的质量,再根据溶质的质量分数求反应后溶液的质量分数.
解答:解:(1)本题中通入足量的H2,在加热条件下进行还原,如果固体产物只有Cu,根据元素守恒,CuO粉末是8.0g,那么铜的质量是:8.0g×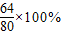 =6.4g,故答案为:6.4g
=6.4g,故答案为:6.4g
(2)固体产物只有铜时,质量是6.4g,第二次反应,冷却后称得固体质量为6.8g,是铜与氧化亚铜的混合物,因此增加的质量是氧元素的质量,氧元素的质量是:6.8g-6.4g=0.4g;根据氧元素的质量求氧化亚铜的质量为:0.4g÷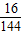 =3.6g.故答案为:0.4g 3.6g
=3.6g.故答案为:0.4g 3.6g
(3)设生成CuCl2的质量为x,生成Cu的质量为y.
Cu2O+2HCl=CuCl2+Cu+H2O
144 135 64
3.6g x y
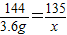 ,x=3.375g
,x=3.375g
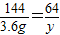 ,y=1.6g
,y=1.6g
w(CuCl2)=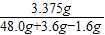 ×100%=6.8%
×100%=6.8%
故答案为:6.8%
点评:本考点既考查了氢气的还原性和质量守恒定律,又考查了根据化学方程式的计算和溶质的质量分数公式的综合应用,通过计算探究物质的组成,是中考的一个重点,也是一个难点.本题考查的知识点比较多,只要认真分析,问题就不难解决.本考点主要出现在填空题和实验题中.
解答:解:(1)本题中通入足量的H2,在加热条件下进行还原,如果固体产物只有Cu,根据元素守恒,CuO粉末是8.0g,那么铜的质量是:8.0g×
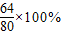 =6.4g,故答案为:6.4g
=6.4g,故答案为:6.4g (2)固体产物只有铜时,质量是6.4g,第二次反应,冷却后称得固体质量为6.8g,是铜与氧化亚铜的混合物,因此增加的质量是氧元素的质量,氧元素的质量是:6.8g-6.4g=0.4g;根据氧元素的质量求氧化亚铜的质量为:0.4g÷
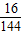 =3.6g.故答案为:0.4g 3.6g
=3.6g.故答案为:0.4g 3.6g (3)设生成CuCl2的质量为x,生成Cu的质量为y.
Cu2O+2HCl=CuCl2+Cu+H2O
144 135 64
3.6g x y
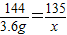 ,x=3.375g
,x=3.375g 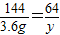 ,y=1.6g
,y=1.6g w(CuCl2)=
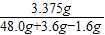 ×100%=6.8%
×100%=6.8%故答案为:6.8%
点评:本考点既考查了氢气的还原性和质量守恒定律,又考查了根据化学方程式的计算和溶质的质量分数公式的综合应用,通过计算探究物质的组成,是中考的一个重点,也是一个难点.本题考查的知识点比较多,只要认真分析,问题就不难解决.本考点主要出现在填空题和实验题中.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目