题目内容
【题目】我国制碱工业先驱侯德榜发明了“侯氏制碱法”。其模拟流程如下:
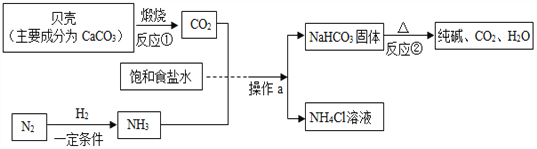
(1)反应的①化学方程式__________________________,反应②的化学方程式__________________________,反应的②基本反应类型为____________。
(2)工业上利用氮气和氧气的__________不同,把氮气液态空气中分离出来。
(3)操作a的名称是___________。
(4)在生产过程中可以循环利用的物质是____________。
【答案】 CaCO3![]() CaO+CO2↑ 2NaHCO3
CaO+CO2↑ 2NaHCO3![]() Na2CO3+CO2↑+H2O 分解反应 沸点 过滤 CO2
Na2CO3+CO2↑+H2O 分解反应 沸点 过滤 CO2
【解析】(1). 碳酸钙在高温条件下分解,生成氧化钙和二氧化碳,反应方程式为:CaCO3![]() CaO+CO2↑ (2).碳酸氢钠在加热条件下分解生成碳酸钠和二氧化碳和水,反应方程式为:2NaHCO3
CaO+CO2↑ (2).碳酸氢钠在加热条件下分解生成碳酸钠和二氧化碳和水,反应方程式为:2NaHCO3![]() Na2CO3+CO2↑+H2O (3). 由一种物质生成两种或两种以上物质的反应是分解反应 (4). (2)工业上利用氮气和氧气的沸点不同,加热时可以先后挥发,把氮气液态空气中分离出来。 (5). 过滤能将难溶性固体 和液体分离 (6). CO2既是生成碳酸氢钠的原料,又是碳酸氢钠分解的产物,可以循环利用。
Na2CO3+CO2↑+H2O (3). 由一种物质生成两种或两种以上物质的反应是分解反应 (4). (2)工业上利用氮气和氧气的沸点不同,加热时可以先后挥发,把氮气液态空气中分离出来。 (5). 过滤能将难溶性固体 和液体分离 (6). CO2既是生成碳酸氢钠的原料,又是碳酸氢钠分解的产物,可以循环利用。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案【题目】在实验课上,同学们将CO2通入到Ca(OH)2溶液中观察到有白色沉淀生成,而将CO2通入到NaOH溶液中无明显现象。
【提出问题】CO2与NaOH溶液是否发生了化学反应?
【提出猜想】CO2与NaOH溶液发生了化学反应
【实验探究】小明设计出了下列4种实验装置,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低。

⑴实验现象为:A中试管内液面上升,B中___________________,C中__________________,D中水槽中的水部分进入烧瓶。
⑵小宁对小明的方案提出了质疑,他认为小明的实验不严谨,其理由是__________________要得到科学严谨的结论,利用方案A,补做的对比实验是_______________________。
⑶小丽的改进方案是利用反应后的溶液来验证猜想,请完成实验报告。
实验操作 | 实验现象 | 实验结论 |
向实验后的溶液中加入稀盐酸 | _______________ | 猜想正确 |
【得出结论】CO2与NaOH溶液发生了化学反应,请写出CO2与NaOH反应的化学方程式:___________________。

