题目内容
芯片的核心部件是以高纯硅(Si)为原料制成的.用化学方法制备高纯硅的化学方程式:X+2H2
Si+4HCl
(1)X的化学式为 .
(2)计算获得56g硅需要氢气的质量.
| ||
(1)X的化学式为
(2)计算获得56g硅需要氢气的质量.
考点:根据化学反应方程式的计算,质量守恒定律及其应用
专题:有关化学方程式的计算
分析:反应前后元素的种类不变,原子的种类、总个数不变;
根据硅的质量可以计算氢气的质量.
根据硅的质量可以计算氢气的质量.
解答:解:(1)由X+2H2
Si+4HCl可知,每个X中含有1个硅原子和4个氯原子,是四氯化硅,化学式是SiCl4.
故填:SiCl4.
(2)设:需要氢气的质量为x,
SiCl4+2H2
Si+4HCl
4 28
x 56g
=
,
x=8g,
答:需要氢气的质量是8g.
| ||
故填:SiCl4.
(2)设:需要氢气的质量为x,
SiCl4+2H2
| ||
4 28
x 56g
| 4 |
| x |
| 28 |
| 56g |
x=8g,
答:需要氢气的质量是8g.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
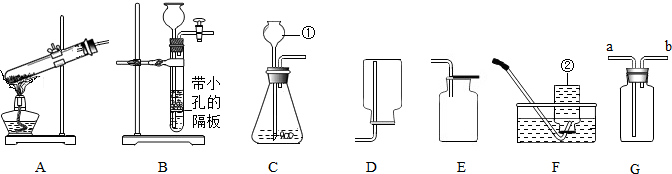
下列实验操作中,正确的是( )
A、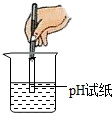 测溶液pH |
B、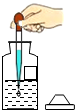 吸取液体药品 |
C、 闻气体的气味 |
D、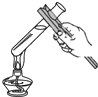 加热液体 |
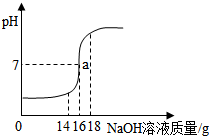 将5%的NaOH溶液逐滴加入到10g稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.边回答:
将5%的NaOH溶液逐滴加入到10g稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.边回答: 人体胃酸过多会引起胃病.如图所示为某抗酸药包装标签上的部分文字,请回答下列问题.
人体胃酸过多会引起胃病.如图所示为某抗酸药包装标签上的部分文字,请回答下列问题.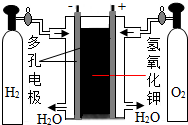 煤、石油、天然气等化石燃料是不可再生能源.植物在光照条件和叶绿素催化作用下发生的光合作用可产生比较丰富的可再生资源,其化学方程式为
煤、石油、天然气等化石燃料是不可再生能源.植物在光照条件和叶绿素催化作用下发生的光合作用可产生比较丰富的可再生资源,其化学方程式为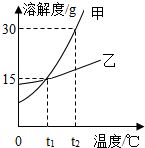 如图为甲、乙两种固体物质的溶解度曲线,请根据图示回答下列问题:
如图为甲、乙两种固体物质的溶解度曲线,请根据图示回答下列问题: