题目内容
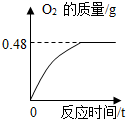
 过氧化氢溶液长期保存会自然分解,使得溶质质量分数减小.小军从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一起测定溶质质量分数.他们取出该溶液51g,加入适量二氧化锰,生成气的质量与反应时间的关系如图所示.
过氧化氢溶液长期保存会自然分解,使得溶质质量分数减小.小军从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一起测定溶质质量分数.他们取出该溶液51g,加入适量二氧化锰,生成气的质量与反应时间的关系如图所示.(l)加入二氧化锰的作用是
催化
催化
.(2)完全反应后生成氧气的质量为
0.48g
0.48g
.(3)计算该溶液中溶质的质量分数.
分析:(1)依据该反应中二氧化锰是催化加分析解答;
(2)由图示可知,完全反应后生成气体的质量为0.48g;
(3)根据过氧化氢溶液分解的化学方程式和生成气体的质量,列出比例式,即可计算出参与反应的H2O2的质量,然后根据质量分数公式计算即可.
(2)由图示可知,完全反应后生成气体的质量为0.48g;
(3)根据过氧化氢溶液分解的化学方程式和生成气体的质量,列出比例式,即可计算出参与反应的H2O2的质量,然后根据质量分数公式计算即可.
解答:解:(1)二氧化锰在该反应中起到催化作用,是该反应的催化剂;
(2)由图象可知完全反应后生成氧气的质量为0.48g;
(3)设参与反应的H2O2的质量为x,
2H2O2
2H2O+O2↑
68 32
x 0.48g
=
解之得:x=1.02g,
该溶液中溶质的质量分数为:
×100%=2%.
故答案为:(1)催化;(2)0.48g;(3)答:该溶液中溶质的质量分数为2%.
(2)由图象可知完全反应后生成氧气的质量为0.48g;
(3)设参与反应的H2O2的质量为x,
2H2O2
| ||
68 32
x 0.48g
| 68 |
| x |
| 32 |
| 0.48g |
解之得:x=1.02g,
该溶液中溶质的质量分数为:
| 1.02g |
| 51g |
故答案为:(1)催化;(2)0.48g;(3)答:该溶液中溶质的质量分数为2%.
点评:本题主要考查学生运用化学方程式和溶质的质量分数公式进行计算的能力,正确识图是解题的关键;

练习册系列答案
相关题目
 2012年“世界水日”的宣传主题是水与链式安全,水是生命之源,我们应该水,爱护水资源.某化学兴趣小组对某地水质状况进行了相关研究调查:
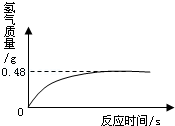
2012年“世界水日”的宣传主题是水与链式安全,水是生命之源,我们应该水,爱护水资源.某化学兴趣小组对某地水质状况进行了相关研究调查: (2011?黄浦区一模)过氧化氢溶液长期保存会分解,使得溶质质量分数减小,张军同学利用校医务室一瓶久置的医用过氧化氢溶液来测定该溶液的溶质质量分数.他们取出该溶液51g,加入适量二氧化锰后生成O2的体积与反应时间的关系如图.(计算时,氧气的密度取1.429g/L)
(2011?黄浦区一模)过氧化氢溶液长期保存会分解,使得溶质质量分数减小,张军同学利用校医务室一瓶久置的医用过氧化氢溶液来测定该溶液的溶质质量分数.他们取出该溶液51g,加入适量二氧化锰后生成O2的体积与反应时间的关系如图.(计算时,氧气的密度取1.429g/L)