题目内容
对于含有68g过氧化氢的双氧水能产生多少克氧气,小海同学利用化学式进行了解答,如表中所示.
(1)请改正小海的错误;
(2)请再用化学方程式计算:68g过氧化氢产生氧气的体积为多少升?(结果保留一位小数,该条件下氧气的密度为1.4g/L)
| 68g过氧化氢中氧元素的质量为: 68g×
氧气中的氧元素来自于过氧化氢,所以68g过氧化氢产生氧气的质量为64g |
(2)请再用化学方程式计算:68g过氧化氢产生氧气的体积为多少升?(结果保留一位小数,该条件下氧气的密度为1.4g/L)
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:过氧化氢分解生成水和氧气,过氧化氢中的氧元素一部分转化到水中,一部分转化到氧气中;
根据过氧化氢的质量可以计算生成氧气的质量,再根据氧气的密度可以计算氧气的体积.
根据过氧化氢的质量可以计算生成氧气的质量,再根据氧气的密度可以计算氧气的体积.
解答:解:(1)小海的错误:过氧化氢中的氧元素完全转化到氧气中,这是不正确的,因为过氧化氢中的氧元素一部分转化到水中,一部分转化到氧气中.
(2)设生成氧气的质量为x,
2H2O2
2H2O+O2↑,
68 32
68g x
=
,
x=32g,
68g过氧化氢产生氧气的体积为:32g÷1.4g/L=22.9L,
答:68g过氧化氢产生氧气的体积为22.9L.
(2)设生成氧气的质量为x,
2H2O2
| ||
68 32
68g x
| 68 |
| 68g |
| 32 |
| x |
x=32g,
68g过氧化氢产生氧气的体积为:32g÷1.4g/L=22.9L,
答:68g过氧化氢产生氧气的体积为22.9L.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 为了加快哈尔滨向现代化大都市迈进的脚步,在市政府的全面规划下,江北、哈西、群力等新城区发展已初具规模.下列有关说法不正确的是( )
为了加快哈尔滨向现代化大都市迈进的脚步,在市政府的全面规划下,江北、哈西、群力等新城区发展已初具规模.下列有关说法不正确的是( )| A、政府部门加强了对“小微”企业的扶持,促进了经济发展 |
| B、城市建设过程中用到的钢材属于金属材料 |
| C、道路建设中设置的护栏大多都喷有油漆,其目的主要为了美观 |
| D、磨盘山引水工程,提高了市民饮用水的质量 |
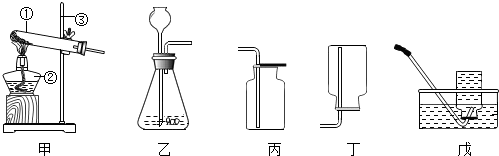
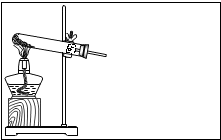 如图是小冰同学正在绘制的实验室用高锰酸钾制取氧气并用排水法收集气体的装置图.请回答下列问题:
如图是小冰同学正在绘制的实验室用高锰酸钾制取氧气并用排水法收集气体的装置图.请回答下列问题: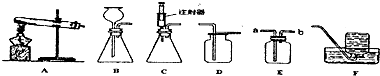
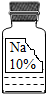 实验室有一瓶常用的无色液体试剂,因保管不当造成标签被损(如图所示),其残缺的标签中剩下其残缺的标签中只剩下“Na”和“10%”字样.小强和小华同学对此很兴趣,决定对其成分进行探究.
实验室有一瓶常用的无色液体试剂,因保管不当造成标签被损(如图所示),其残缺的标签中剩下其残缺的标签中只剩下“Na”和“10%”字样.小强和小华同学对此很兴趣,决定对其成分进行探究.