题目内容
【题目】溶液在日常生活和生产中应用广泛,请回答下列问题;
(1)糖水、生理盐水、白酒都是溶液。它们的共同点是:、、混合物。
(2)写出下列溶液中溶质的化学式:盐酸、澄清石灰水、碘酒、
(3)K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下:
温度/℃ | 20 | 30 | 50 | 60 | 80 | |
溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |
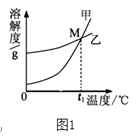

① 图1中能表示KNO3溶解度曲线的是(填“甲”或“乙”)。
② 若甲中混有少量的乙,最好采用方法提纯甲
(4)60℃时,向两个分别盛有相同质量的K2CO3和KNO3的烧杯中,各加入100g水,充分溶解后,恢复至60℃,其结果如图2所示。则烧杯①中的溶质是 , 此时烧杯①溶液的溶质质量分数为。
【答案】
(1)均一性,稳定性
(2)HCl,Ca(OH)2,I2
(3)甲,冷却热饱和溶液/降温结晶
(4)KNO3,52.4%
【解析】(1)糖水、生理盐水、白酒都是溶液。它们的共同点是∶均一性,稳定性,混合物。
(2)溶液中溶质的化学式:盐酸HCl、澄清石灰水是Ca(OH)2、碘酒是I2 。
(3)因为KNO3溶解度受温度影响较大,所以① 图1中能表示KNO3溶解度曲线的是甲。② 若甲中混有少量的乙,最好采用冷却热饱和溶液/降温结晶方法提纯甲,因为甲溶解度受温度影响较大,乙溶解度受温度影响变化不大。
(4)60℃时,向两个分别盛有相同质量的K2CO3和KNO3的烧杯中,各加入100g水,充分溶解后,恢复至60℃,其结果如图2所示。则烧杯①中的溶质是KNO3 ,60℃时K2CO3 溶解度大于KNO3 溶解度,此时烧杯①溶液的溶质质量分数为∶ ![]() ×100%=52.4%。
×100%=52.4%。
【考点精析】解答此题的关键在于理解饱和溶液和不饱和溶液相互转变的方法的相关知识,掌握饱和和不饱和的转变方法:①Ca(OH)2和气体等除外,它的溶解度随温度升高而降低②最可靠的方法是:加溶质、蒸发溶剂,以及对固体溶解度曲线及其作用的理解,了解1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和).