题目内容
(2010?武汉)现有甲、乙两包白色固体,已知甲中含有NaCl、NaNO3、Na2CO3、NaOH中的一种或几种,乙为纯净物,是初中化学学习中涉及到的物质.为了证明甲、乙两包固体的成分,现进行如下实验:
(1)实验一
(2)实验二(部分物质在流程图中未列出)

根据以上实验推断,乙物质为
(1)实验一
| 操作步骤 | 实验现象 | 结论 |
| ①取甲中少量粉末加足量水充分溶解 | 溶液呈无色 | 甲中含有NaCl、NaNO3、Na2CO3、NaOH中的一种或几种 甲中含有NaCl、NaNO3、Na2CO3、NaOH中的一种或几种 |
| ②取①中所得溶液少量,滴加紫色石蕊试液 | 石蕊试液变了蓝色 | 溶液pH > > 7(填“>”、“<”或“=” |
| ③另取①中所得溶液少量,滴加稀盐酸 | 无明显现象 |
甲中一定含有 NaOH NaOH (填化学式,下同),一定不含Na2CO3 Na2CO3 ,可能含有NaCl、NaNO3 NaCl、NaNO3 . |

根据以上实验推断,乙物质为
(NH4)2SO4
(NH4)2SO4
(填写化学式),使用该物质时应注意不能与碱性物质混用
不能与碱性物质混用
.分析:根据题意,加入石蕊试液变蓝色,说明溶液呈碱性,则pH>7,而Na2CO3、NaOH均呈碱性,加稀盐酸后无明显现象,说明混合物中一定不含Na2CO3,则一定含有NaOH.对于NaCl、NaNO3没有进行验证,所以均可能含有.
解答:解:(1)实验一:根据题意,加入石蕊试液变蓝色,说明溶液呈碱性,则pH>7,而Na2CO3、NaOH均呈碱性,加稀盐酸后无明显现象,说明混合物中一定不含Na2CO3,则一定含有NaOH.对于NaCl、NaNO3没有进行验证,所以均可能含有.
(2)实验二:根据图可知,气体通入澄清酚酞溶液,溶液变红,则可知为碱性气体:氨气;而所得无色溶液与硝酸钡溶液反应生成不溶于硝酸的白色沉淀,则可推测为硫酸钡沉淀;故根据以上实验推断,乙物质为 (NH4)2SO4(填写化学式),使用该物质时应注意不能与碱性物质混用.
故答为:(1)②>;③NaOH; NaCO3;NaCl、NaNO3
(2)(NH4)2SO4; 不能与碱性物质混用(答具体的物质或碱均可)
| 操作步骤 | 实验现象 | 结论 |
| ①取甲中少量粉末加足量水充分溶解 | 溶液呈无色 | 甲中含有NaCl、NaNO3、NaCO3、NaOH中的一种或几种 |
| ②取①中所得溶液少量,滴加紫色石蕊试液 | 石蕊试液变了蓝色 | 溶液pH>7(填“>”、“<”或“=” |
| ③另取①中所得溶液少量,滴加稀盐酸 | 无明显现象 |
甲中一定含有 NaOH(填化学式,下同),一定不含 NaCO3,可能含有 NaCl、NaNO3. |
故答为:(1)②>;③NaOH; NaCO3;NaCl、NaNO3
(2)(NH4)2SO4; 不能与碱性物质混用(答具体的物质或碱均可)
点评:解答此类试题,需要学生有较强的逻辑推理和分析能力.但这些能力并不能够凭空生成,需要建构好相关的知识结构.如对常见物质的溶解性、颜色、俗称的熟练掌握是基本功,对复分解反应能否发生的判断是解答的关键,还包括对实验设计的合理评价,现象的准确描述,结论的准确判断等科学素养的综合体现.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
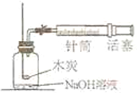 (2010?武汉)燃料燃烧所产生的热量给生活与生产带来了很大的便利,但燃烧不当也会造成极大的损害.
(2010?武汉)燃料燃烧所产生的热量给生活与生产带来了很大的便利,但燃烧不当也会造成极大的损害.