题目内容
下图是“×××”钙片商品标签图.你能根据标签信息完成下列两题吗?
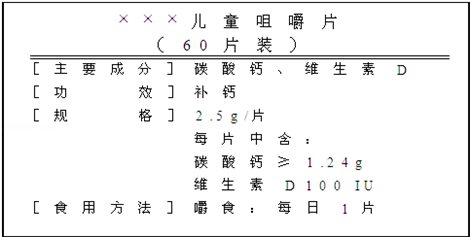
(1)主要成分碳酸钙的相对分子质量为 _________ ;每片中至少含钙元素的质量为 _________ g.(保留两位有效数字)
(2)小蓉同学为测定其碳酸钙的含量标注是否属实,她取出4片片剂,研碎后放入烧杯中,逐滴加入稀盐酸,至不再放出气体为止,共用去稀盐酸40.0g,称量烧杯中剩余物质的质量为47.8g(不含烧杯质量,假定钙片其他成分不与盐酸反应.)(反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑)请求出:
①生成二氧化碳的质量;
②稀盐酸中溶质的质量分数(精确到0.01);
(3)通过计算判断钙片中碳酸钙的含量标注是否属实.
(2)小蓉同学为测定其碳酸钙的含量标注是否属实,她取出4片片剂,研碎后放入烧杯中,逐滴加入稀盐酸,至不再放出气体为止,共用去稀盐酸40.0g,称量烧杯中剩余物质的质量为47.8g(不含烧杯质量,假定钙片其他成分不与盐酸反应.)(反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑)请求出:
①生成二氧化碳的质量;
②稀盐酸中溶质的质量分数(精确到0.01);
(3)通过计算判断钙片中碳酸钙的含量标注是否属实.
(1)100;0.50.
(2)解:①根据质量守恒定律可知,生成CO2的质量为:40g+4×2.5g﹣47.8g=2.2g
②设参加反应的CaCO3和HCl的质量分别为x,y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
x y 2.2g

解得y=3.65g
则稀盐酸中溶质的质量分数为: ×100%=9.13%.
×100%=9.13%.
(3)
解得:x=5g;
每片含CaCO3的质量为: =1.25g>1.24g,
=1.25g>1.24g,
故钙片中碳酸钙的含量标注准确.
答:生成二氧化碳的质量是2.2g,稀盐酸中溶质的质量分数为9.13%,通过计算含量标注属实.
(2)解:①根据质量守恒定律可知,生成CO2的质量为:40g+4×2.5g﹣47.8g=2.2g
②设参加反应的CaCO3和HCl的质量分别为x,y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
x y 2.2g

解得y=3.65g
则稀盐酸中溶质的质量分数为:
 ×100%=9.13%.
×100%=9.13%.(3)

解得:x=5g;
每片含CaCO3的质量为:
 =1.25g>1.24g,
=1.25g>1.24g,故钙片中碳酸钙的含量标注准确.
答:生成二氧化碳的质量是2.2g,稀盐酸中溶质的质量分数为9.13%,通过计算含量标注属实.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
?下图是“×××”补钙商品标签图.请根据标签信息完成下列两题:
(1)每片药剂中至少含钙元素的质量为 g.
(2)小明为测定其碳酸钙的含量标注是否属实,他取出4片片剂,研碎后放入烧杯中,逐滴加入稀盐酸,至不再放出气体为止,共用去稀盐酸40.0g,称量烧杯中剩余物质量为47.8g(不含烧杯质量,假定钙片其他成分不与盐酸反应.)通过计算判断钙片中碳酸钙的含量标注是否属实.
| ×××儿童咀嚼片 (60片装) [主要成分]碳酸钙、维生素D |
| [功效]补钙 [规格]25g/片 每片中含: 碳酸钙≥124g 维生素D100IU [食用方法]嚼食.每日1片 |
(2)小明为测定其碳酸钙的含量标注是否属实,他取出4片片剂,研碎后放入烧杯中,逐滴加入稀盐酸,至不再放出气体为止,共用去稀盐酸40.0g,称量烧杯中剩余物质量为47.8g(不含烧杯质量,假定钙片其他成分不与盐酸反应.)通过计算判断钙片中碳酸钙的含量标注是否属实.



