题目内容
某课外学习小组对过氧化氢的分解反应进行探究,实验条件及产生的现象见下表:
| 实验序号 | 实验温度/0C | 催化剂 | 5%H2O2溶液体积/mL | 实验现象 |
| (1) | 20 | 无 | 10 | 无明显现象 |
| (2) | 50 | 无 | 10 | 有气泡产生 |
| (3) | 20 | 1gCuCl2 | 10 | 有气泡产生 |
| (4) | 20 | 1gFeCl3 | 10 | 有气泡产生[快慢与(3)不同] |
(资料显示Na+、SO42-对此反应无催化作用)根据以上信息回答下列问题:
(1)写出实验(4)的化学方程式 ;
(2)实验(1)与(2)的目的是探究 ;
(3)实验(3)与(4)的目的是探究 ;
(4)为了进一步探究FeCl3在溶液中起催化作用的是什么离子,还应进一步设计实验,请根据提出的假设填写所需试剂;
| 提出假设 | 除H2O2外至少还需选用的试剂 |
| 假设l:只有Fe3+有催化作用 | ① |
| 假设2:只有Cl-有催化作用 | ② |
| 假设3:Fe3+ 、Cl一都有催化作用 | ③ |

(5)为了证明FeCl3是该反应的催化剂,还需:
①验证FeCl3在反应前后质量不变;
②验证 。
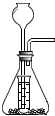
(6)小明用H2O2和MnO2按右图装置制取少量的O2,其中小试管的作用是
。(填2种即可)
(1)
(2)其他条件相同的情况下,温度对过氧化氢速率的影响·········2分
(3)其他条件相同的情况下,不同的催化剂对H2O2分解速率影响的差异···2分
(4)①NaCl································1分
②Fe2(SO4)3································1分
③NaCl和Fe2(SO4)3·····························1分
(5)FeCl3在反应前后化学性质保持不变···············1分
(6)节约试剂;防止气体从长颈漏斗逸出;便于控制反应·······2分

| 实验序号 | 实验温度/℃ | 催化剂 | 5%H2O2溶液体积/mL | 实验现象 |
| (1) | 20 | 无 | 10 | 无明显现象 |
| (2) | 50 | 无 | 10 | 有气泡产生 |
| (3) | 20 | 1gCuCl2 | 10 | 有气泡产生 |
| (4) | 20 | 1gFeCl3 | 10 | 有气泡产生(快慢与(3)不同) |
 对此反应无催化作用)
对此反应无催化作用)根据以上信息回答下列问题:
(1)写出实验(4)的化学方程式______ 2H2O+O2↑