题目内容
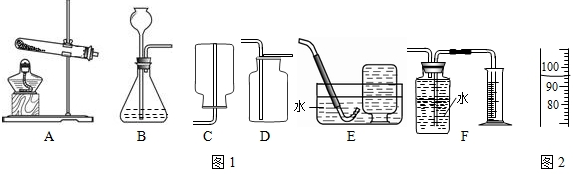
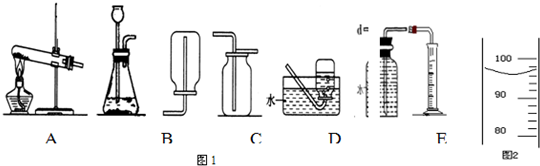
氢气是最轻的气体,难溶于水.氢气作为未来的理想能源,是航天工业的高能燃料,也是化工生产的重要原料.实验室通常采用下面装置制取少量氢气,
请根据要求回答:
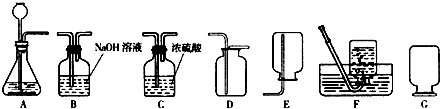
①实验室使用稀盐酸和金属锌制取氢气的化学反应方程式为______,这种方法制得的氢气往往含有少量HCl和水蒸气,可将杂质气体通过装置B除去,其原理用化学方程式表示______
②实验中可采用______装置收集氢气;集满氢气后的集气瓶按装置G方式放置备用,原因是______.
【答案】分析:①从锌与稀盐酸反应生成氯化锌及氢气分析书写方程式,根据B装置中氢氧化钠的性质分析除掉的杂质;
②根据氢气的物理性质特别是密度比空气小以及难溶于水分析判断.
解答:解:①锌与稀盐酸反应生成氯化锌及氢气,其方程式为Zn+2HCl=ZnCl2+H2↑;由于B装置中氢氧化钠能与氯化氢反应,所以可除掉气体中的氯化氢气体,其方程式为:HCl+NaOH=NaCl+H2O;
②由于氢气密度比空气小,所以可采用向下排空气法收集,且集满氢气后的集气瓶应倒放到桌面上,氢气难溶于水,所以也可采用排水法收集;
故答案为:①Zn+2HCl=ZnCl2+H2↑;HCl+NaOH=NaCl+H2O;②E、F; 因为氢气的密度比空气小.
点评:此题是对氢气制取及除杂的考查,解题的关键是掌握相关物质的性质,属基础性知识考查题.
②根据氢气的物理性质特别是密度比空气小以及难溶于水分析判断.
解答:解:①锌与稀盐酸反应生成氯化锌及氢气,其方程式为Zn+2HCl=ZnCl2+H2↑;由于B装置中氢氧化钠能与氯化氢反应,所以可除掉气体中的氯化氢气体,其方程式为:HCl+NaOH=NaCl+H2O;
②由于氢气密度比空气小,所以可采用向下排空气法收集,且集满氢气后的集气瓶应倒放到桌面上,氢气难溶于水,所以也可采用排水法收集;
故答案为:①Zn+2HCl=ZnCl2+H2↑;HCl+NaOH=NaCl+H2O;②E、F; 因为氢气的密度比空气小.
点评:此题是对氢气制取及除杂的考查,解题的关键是掌握相关物质的性质,属基础性知识考查题.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目