题目内容
【题目】为进一步认识氧气,老师邀请你参加实验室制取氧气实践和研究. 
(1)写出一个实验室用装置A制取氧气的化学反应文字表达式是 . 该反应属于反应(填化学反应基本类型)
(2)在加热氯酸钾制O2的过程中,发现产生O2的速率很慢,经检查氯酸钾未变质,装置气密性良好,你认为最可能的原因是 .
(3)与A相比,用B装置制取氧气的优点有 .
A.安全
B.节约能源
C.不用检查气密性
D.环保,污染少
(4)实验室利用锌粒与稀硫酸在常温下反应制取氢气,发生装置可选择图中的 . 用D装置收集氢气,氢气应该从端通入(填“a”或“b”).
(5)如图E,为检查装置的气密性,保持装置内温度不变,将导管末端伸入装有水的烧杯中.若装置气密性良好,烧杯内导管处的现象(图中烧杯内画圈部分)是表中的
选项 | A | B | C | D |
现象放大图 |
|
|
|
|
【答案】
(1)高锰酸钾 ![]() 锰酸钾+二氧化锰+氧气;分解
锰酸钾+二氧化锰+氧气;分解
(2)没有加MnO2
(3)ABD
(4)B;a
(5)B
【解析】解:(1)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,属于分解反应;所以答案是:高锰酸钾 ![]() 锰酸钾+二氧化锰+氧气;分解(2)在加热氯酸钾制O2的过程中,发现产生O2的速率很慢,经检查氯酸钾未变质,装置气密性良好,我认为最可能的原因是没有加MnO2;所以答案是:没有加MnO2(3)与A相比,用B装置制取氧气的优点有:安全、节约能源、环保,污染少;所以答案是:ABD (4)实验室是用锌粒和稀硫酸在常温下反应制氢气的,因此不需要加热;用D装置收集氢气,氢气应该从a端通入,因为氢气的密度比空气的密度小.所以答案是:B;a(5)检验装置的气密性的方法是:先把导管的一端放入水中,然后两手紧握试管的外壁,观察导管口是否有气泡冒出;所以答案是:B
锰酸钾+二氧化锰+氧气;分解(2)在加热氯酸钾制O2的过程中,发现产生O2的速率很慢,经检查氯酸钾未变质,装置气密性良好,我认为最可能的原因是没有加MnO2;所以答案是:没有加MnO2(3)与A相比,用B装置制取氧气的优点有:安全、节约能源、环保,污染少;所以答案是:ABD (4)实验室是用锌粒和稀硫酸在常温下反应制氢气的,因此不需要加热;用D装置收集氢气,氢气应该从a端通入,因为氢气的密度比空气的密度小.所以答案是:B;a(5)检验装置的气密性的方法是:先把导管的一端放入水中,然后两手紧握试管的外壁,观察导管口是否有气泡冒出;所以答案是:B
【考点精析】利用检查装置的气密性和氧气的制取装置对题目进行判断即可得到答案,需要熟知装置气密性检查:先将导管的一端浸入水中,用手紧贴容器外壁,稍停片刻,若导管口有气泡冒出,松开手掌,导管口部有水柱上升,稍停片刻,水柱并不回落,就说明装置不漏气;发生装置:固固加热型、固液不加热型.

 一本好题口算题卡系列答案
一本好题口算题卡系列答案【题目】在宏观、微观和符号之间建立联系是化学学科的特点.
(1)按要求填写指定的化学符号或符号的意义
化学符号 | 2N | 3SO42﹣ | |
符号的意义 | 2个氧分子 |
(2)如图1是1一18号元素中部分粒子的结构示意图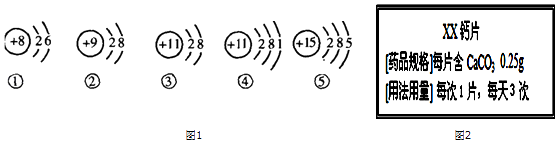
其中属于同种元素的是(填序号);属于阴离子的是;(用粒子符号表示)①和④两种元素组成的化合物的化学式是;⑤的原子核内的中子数比核外电子数多1个,则它的相对原子质量是 .
(3)在一个化学反应中,如果有元素化合价升高,同时就有元素化合价降低.探究钠元素的单质与水反应的生成物.甲同学猜想生成物为NaOH和H2;乙同学猜想生成物为NaOH和O2 , 经过讨论后,大家一致认为乙同学的猜想不合理,请从化合价的角度解释原因 .
(4)钙元素对人体健康很重要,是人体必须的常量元素,每日必须摄入足够量的钙.目前市场上的补钙药剂很多,图2是某种品牌的补钙药品的部分说明书.请回答下列问题:
①CaCO3中碳、氧元素的质量比是 .
②CaCO3中钙元素的质量分数为 .
③如果按用量服用,每天摄入钙元素的质量为 g.