题目内容
【题目】根据下图回答问题:
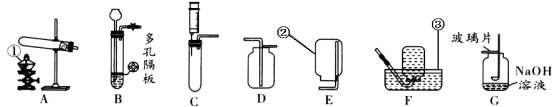
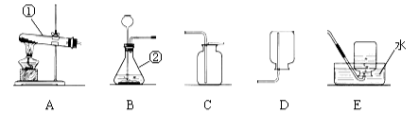
(1)写出图中标号仪器名称:③ 。
(2)实验室用高锰酸钾制取氧气制取装置 (填序号),反应文字表达式为 。检验装置气密性时,除了用手紧握的方法外,还可以采用的方法是 ;
(3)实验室可用二氧化锰固体与过氧化氢溶液在常温下混合制取氧气,为了得到平稳的氧气流,应选择的发生装置是 ;反应文字表达式为: 。
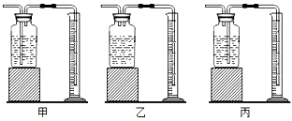
(4)用N装置做硫在氧气中燃烧实验,燃烧结束后取出燃烧匙,立即用玻璃片盖住并震荡(注氢氧化钠会与二氧化硫反应),若将集气瓶倒转,发现玻璃片被吸住而掉不下来(如甲图),其原因是 ;
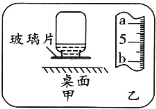
(5)为完成上述实验,用10mL量筒量取6mL氢氧化钠溶液,读数时量筒内的液体凹液面最低处与乙图中 处(填a或b)刻度线保持水平。
(6)在实验室中,集气瓶被称做“万能瓶”,用它可以组装成各种用途的装置,请仔细观察下列(F~K)各个装置的特点回答问题:

①实验室若用F装置收集氧气,则氧气应从________口进入(填导管口符号).
②若要收集一定体积的二氧化碳气体,应选用________装置.
③若要除去一氧化碳中的少量二氧化碳,同时用该瓶收集较纯净的一氧化碳,应选用__________装置.
【答案】(1) 水槽
(2)AD或AM 高锰酸钾![]() 锰酸钾+二氧化锰+氧气 用酒精灯加热试管
锰酸钾+二氧化锰+氧气 用酒精灯加热试管
(3)C 过氧化氢 → 水+氧气
(4)氢氧化钠和二氧化硫反应,使瓶中压强减小,大气压压着玻璃片不掉下
(5)a(6)①b ②K ③H
【解析】
试题分析∶由题中信息和所学知识知,(1)图中标号仪器名称:③水槽。(2)实验室用高锰酸钾制取氧气制取装置AD或AM。反应文字表达式为高锰酸钾![]() 锰酸钾+二氧化锰+氧气。检验装置气密性时,除了用手紧握的方法外,还可以采用的方法是用酒精灯加热试管。(3)实验室可用二氧化锰固体与过氧化氢溶液在常温下混合制取氧气,为了得到平稳的氧气流,应选择的发生装置是C,反应文字表达式为:过氧化氢→水+氧气。(4)用N装置做硫在氧气中燃烧实验,燃烧结束后取出燃烧匙,立即用玻璃片盖住并震荡(注氢氧化钠会与二氧化硫反应),若将集气瓶倒转,发现玻璃片被吸住而掉不下来(如甲图),其原因是氢氧化钠和二氧化硫反应,使瓶中压强减小,大气压压着玻璃片不掉下。(5)为完成上述实验,用10mL量筒量取6mL氢氧化钠溶液,读数时量筒内的液体凹液面最低处与乙图中a处刻度线保持水平。⑹①①实验室若用F装置收集氧气,则氧气应从b口进入.②②若要收集一定体积的二氧化碳气体,应选用k装置.③③若要除去一氧化碳中的少量二氧化碳,同时用该瓶收集较纯净的一氧化碳,应选用H装置.
锰酸钾+二氧化锰+氧气。检验装置气密性时,除了用手紧握的方法外,还可以采用的方法是用酒精灯加热试管。(3)实验室可用二氧化锰固体与过氧化氢溶液在常温下混合制取氧气,为了得到平稳的氧气流,应选择的发生装置是C,反应文字表达式为:过氧化氢→水+氧气。(4)用N装置做硫在氧气中燃烧实验,燃烧结束后取出燃烧匙,立即用玻璃片盖住并震荡(注氢氧化钠会与二氧化硫反应),若将集气瓶倒转,发现玻璃片被吸住而掉不下来(如甲图),其原因是氢氧化钠和二氧化硫反应,使瓶中压强减小,大气压压着玻璃片不掉下。(5)为完成上述实验,用10mL量筒量取6mL氢氧化钠溶液,读数时量筒内的液体凹液面最低处与乙图中a处刻度线保持水平。⑹①①实验室若用F装置收集氧气,则氧气应从b口进入.②②若要收集一定体积的二氧化碳气体,应选用k装置.③③若要除去一氧化碳中的少量二氧化碳,同时用该瓶收集较纯净的一氧化碳,应选用H装置.
考点∶考查化学实验的基本操作。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案【题目】为测定某BaCl2溶液的溶质质量分数,进行如下实验:取104g该溶液于烧杯中,加入1g稀硝酸溶液酸化,无任何现象,然后将30g一定溶质质量分数的硫酸溶液分三次加入,每次充分反应后过滤、称量(实验中物质的质量损失忽)不计),数据如表:
第1次 | 第2次 | 第3次 | |
加入硫酸溶液的质量/g | 10 | 10 | 10 |
过滤后溶液的质量/g | 105 | 105 | 111.7 |
根据以上数据计算:(BaCl2+H2SO4═BaSO4↓+2HCl)
(1)该实验过程中产生沉淀的总质量为 g.
(2)该BaCl2溶液中溶质的质量分数(写出计算过程)
【题目】小明同学在家里的药箱中发现一瓶用来清洗伤口用的消毒液——“双氧水”,他联想到在化学课上曾用过氧化氢溶液制取过氧气,他高兴的将家中的“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验。

【第一组实验】小明欲证明该双氧水是否失效。
(1)实验过程
①在试管中加入5 mL “双氧水”,把带火星的木条伸入试管中,发现木条未复燃;
②用酒精灯给上述试管加热,液体中有气泡产生,把带火星的木条伸入试管中,发现木条仍未复燃;
③如图装置进行操作,带火星的木条复燃,水槽中冰水所起的作用是 。
(2)实验结论: 。
【第二组实验】小明欲探究Fe2O3能否作为H2O2分解的催化剂,并与MnO2的催化效果进行比较。小明、小李、小张三位同学同时进行H2O2的分解与气体的收集实验。实验时间均以30秒生成气体为准(H2O2均未全部分解)(见图甲),其他可能影响实验的因素均忽略。相关数据如下:


同学序号 | 质量分数相同的H2O2溶液 | 溶液中加入的物质 | 收集到的气体体积 |
小明 | 100 ml | 未加其他物质 | a ml |
小李 | 100 ml | Fe2O3 0.5 g | b ml |
小张 | 100 ml | MnO2 0.5 g | c ml |
(1)若50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A为20,则此时气体的体积为 mL。
(2)欲探究Fe2O3在实验中是否起催化作用,首先应比较 和 (选择a、b、c填空)的大小,还需补充做如下实验(无需写出具体操作步骤):
① ;
② 。
实验结论:Fe2O3能加快H2O2的分解,起催化作用。
(3)通过比较Fe2O3 和MnO2 在反应中的反应速率,发现Fe2O3 的催化效果没有二氧化锰好。