题目内容
【题目】生产、生活、科技、环保等都离不开化学
(1)能源、环境与人类的生活和社会发展密切相关。
①目前,人类以化石燃料为主要能源,常见的化石燃料包括煤、石油和_____。
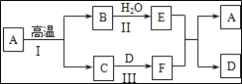
②为减少污染、提高煤的利用率,可将其转化为可燃性气体水煤气,此过程可认为是碳与水的反应,其微观示意图如下所示:
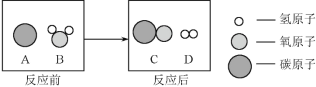
该反应的基本反应类型为_____;该反应生成物的分子个数比为_____。
③水煤气在不同催化剂作用下,可以合成不同物质,如重要有机物甲醇(CH3OH),写出该反应的化学方程式_____。有人认为仅利用水煤气在催化剂作用下不能合成尿素〔CO(NH2)2〕,理由是_____。
(2)糖类、油脂、蛋白质都是人体必需的营养物质,合理膳食是健康的基本保证。
①食物的成分主要有蛋白质、_____、油脂、维生素、无机盐和水等六大类,通常称为营养素。下列食品中富含蛋白质的是_____(填写序号)。
A菠菜 B鸡蛋 C花生油 D米饭E牛奶
②黄瓜中富含维生素C,维生素C在pH<5和低温的环境中较稳定,为减少维生素C的损失,食用黄瓜的最佳方法是_____。
(3)材料是人类赖以生存的重要物质基础。材料种类很多,通常可分为金属材料、无机非金属材料、高分子合成材料及复合材料。
①铁锅、铝锅、铜锅用来炒菜、做饭是利用了它们的_____。金属的使用早晚与其活动性有着密切的关系。利用下列试剂与上面三种金属来探究它们的金属活动性顺序,能达到目的是_____(填序号)。
A硫酸铝溶液 B.硫酸亚铁溶液 C硫酸铜溶液
②下列有关合金性质的说法正确的是_____(填字母)。
A合金的熔点一般比它的成分金属高
B合金的硬度一般比它的成分金属低
C组成合金的元素种类相同,合金的性能就一定相同
D合金与各成分金属相比,具有许多优良的物理、化学或机械性能
③下列对金属制品采取的防护方法不正确的是_____(填序号)。
A在电线的外面包上一层塑料层 B在自行车钢圈上镀上一层金属铬 C在海轮的铁制外壳上焊上铜
④合成塑料、合成橡胶和_____是常说的三大合成材料。下列制品中含有合成橡胶的是_____(填字母)。
A汽车轮胎 B涤纶 C聚氯乙烯制品 D玻璃钢
【答案】天然气 置换反应 1:1  水煤气中不含氮元素,不可能合成含氮元素的尿素 糖类 BE 加少量食醋,凉拌 导热性 B D C 合成纤维 A
水煤气中不含氮元素,不可能合成含氮元素的尿素 糖类 BE 加少量食醋,凉拌 导热性 B D C 合成纤维 A
【解析】
(1)①目前,人类以化石燃料为主要能源,常见的化石燃料包括煤、石油和天然气;
②根据图示可知,此反应是:C+H2O![]() CO+H2,该反应是由一种单质与一种化合物反应生成另一种单质与另一种化合物,属于置换反应,由化学方程式可知,该反应生成物的分子个数比为1:1;
CO+H2,该反应是由一种单质与一种化合物反应生成另一种单质与另一种化合物,属于置换反应,由化学方程式可知,该反应生成物的分子个数比为1:1;
③根据信息:水煤气(CO和H2)在催化剂作用下,可以合成有机物甲醇(CH3OH)。化学方程式是:CO+2H2![]() CH3OH.水煤气中不含有氮元素而尿素中含有氮元素,根据化学反应前后元素种类不变,反应物中没有氮元素,故不能得到尿素。仅利用水煤气在催化剂作用下不能合成尿素〔CO(NH2)2〕,理由是水煤气中不含氮元素,不可能合成含氮元素的尿素。
CH3OH.水煤气中不含有氮元素而尿素中含有氮元素,根据化学反应前后元素种类不变,反应物中没有氮元素,故不能得到尿素。仅利用水煤气在催化剂作用下不能合成尿素〔CO(NH2)2〕,理由是水煤气中不含氮元素,不可能合成含氮元素的尿素。
(2)①人体所需的营养元素有:蛋白质、糖类、油脂、维生素、无机盐和水等六大类,鸡蛋和牛奶中含有大量的蛋白质,故选BE;
②由于维生素C在pH<5和低温的环境中较稳定,所以在吃黄瓜时,加少量食醋,凉拌;
(3)①铁锅、铝锅、铜锅用来炒菜、做饭是利用了它们的导热性。金属的使用早晚与其活动性有着密切的关系。要探究三种金属的活动性顺序,可选择金属铝、铜和硫酸亚铁溶液来进行验证。铝能与硫酸亚铁反应生成硫酸铝和铁,说明铝的活动性大于铁,铜不能与硫酸亚铁反应,说明铁的活动性大于铜,两个实验能三种金属的活动性顺序是铝>铁>铜。故选B;
②A合金的熔点一般比它的成分金属低,故A错误;
B合金的硬度一般比它的成分金属高,故B错误;
C 组成合金的元素种类不同,但合金中各元素的含量不同,合金的性能就不一样,例如生铁和钢,合金的性能可以通过所添加的元素的种类、含量和生成合金的条件等来加以控制,故C错误;
D 合金与各组成金属相比,合金的熔点比它的各成分金属的熔点都低,硬度比它的各成分金属的大,机械性能好,有些金属具有较强的抗腐蚀性,故D正确。故选D;
③A 外面包上一层塑料层可减少与空气中氧气的接触,故A正确;
B 镀上一层金属铬可以隔绝空气,使金属不受腐蚀,故B正确;
C 原电池能加快化学反应速率,铁铜海水构成原电池,加快铁的腐蚀,故C错误。故选C;
④人们通常所说的三大合成材料是指塑料、合成纤维、合成橡胶;汽车轮胎是由合成橡胶和金属材料制成的复合材料,涤纶是合成纤维,聚乙烯制品是塑料,玻璃钢是无机复合材料。故选A。

 名校课堂系列答案
名校课堂系列答案