题目内容
【题目】用金属铁通过一系列转化,可以制备新型消毒、净水剂K2FeO4.流程如下:
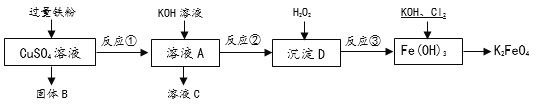
请回答下列问题:
(1)固体B的成分是_____________(用化学式表示);反应①后经过__________操作可分别得到固体B和溶液A.
(2)反应①、②、③中没有涉及到的化学基本反应类型是__________.
(3)请写出反应②的化学方程式___________________________.
(4)如果所得净水剂K2FeO4的质量为19.8kg,则理论上参加反应的铁的质量为____kg.
【答案】 Cu、Fe 过滤 分解反应 FeSO4+2KOH= Fe(OH)2↓+K2SO4 5.6
【解析】(1)根据过量铁粉与硫酸铜溶液的反应分析固体B的成分;根据过滤的原理及操作过程分析解答;
(2)根据发生的反应及反应的特点,分析没有涉及的反应类型;
(3)根据发生的反应写出反应的化学方程式;
(4)根据反应的关系解答。
解:(1)由反应流程可知,过量铁粉与硫酸铜溶液反应,生成硫酸亚铁和铜,由于铁是过量的,在过滤后得到的固体B是Cu、Fe的混合物; 反应①后得到 固体B和溶液A。故进行的操作是过滤;
(2)由反应流程可知,反应①是Fe+CuSO4=Cu+FeSO4,属于置换反应;反应②是FeSO4+2KOH=Fe(OH)2↓+K2SO4,属于复分解反应;反应③是2Fe(OH)2+H2O2= 2Fe(OH)3,属于化合反应。故反应①、②、③中没有涉及到的化学基本反应类型是:分解反应;
(3)反应②的化学方程式:FeSO4+2KOH= Fe(OH)2↓+K2SO4;
(4)根据分析可知,K2FeO4中铁元素的质量来自参加反应的铁的质量。设参加反应的铁的质量为x。
Fe ~ K2FeO4
56 198
x 19.8g
![]()
x=5.6kg。

 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案