题目内容
【题目】某兴趣小组对物质的性质和成分进行相关探究.
(1)常见金属活动性顺序如下,填写想用的元素符号: ![]()
某同学用硫酸铜溶液把“把铁刀变成铜刀”,其反应的化学方程式为 , 该反应的基本反应类型为 .
(2)将一定质量的锌粒投入含有Cu(NO3)2和Fe(NO3)2的混合溶液中,充分反应后过滤,则滤渣中一定含有 , 可能含有 .
(3)兴趣小组同学用氧化铜与足量的炭粉利用图甲所示装置进行实验,对生成气体的成分进行探究. 
【提出问题】生成的气体中是否含有一氧化碳?
【实验与讨论】
①打开K,缓缓通入干燥的氮气一段时间.
②关闭K,加热至一定温度使之反应,用气囊收集气体样品.
③除去气体样品中的二氧化碳,并将剩余气体收集在集气瓶中,下列装置中最为合理的是(填字母).(注:氢氧化钠能与CO2反应,但不能与CO反应,CO2的密度约为1.5g/l,CO的密度约为4.25g/l)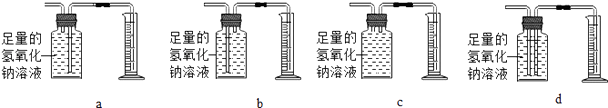
【实验求证】
将除尽二氧化碳后的气体样品干燥,仍然用图甲所示的装置进行实验,A中的固体应选用 , B中溶液为澄清石灰水,若A中黑色固体出现了红色,B中澄清石灰水 , 可说明气体样品中含有一氧化碳.
【答案】
(1)Fe+CuSO4=Cu+FeSO4;置换反应
(2)铜;铁,锌
(3)d;氧化铜;变浑浊
【解析】解:(1)由金属的活动性顺序为K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au可知,在金属活动顺序表空格内应填入Mg、Ag;铁与硫酸铜溶液反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4=Cu+FeSO4;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应;(2)锌会与硝酸铜、硝酸亚铁反应生成硝酸锌、铜、铁,将一定质量的锌粒投入含有Cu(NO3)2和Fe(NO3)2的混合溶液中,充分反应后过滤,若滤液中只含一种溶质,应该是硝酸锌,所以滤渣中一定含有铜、铁;
【考点精析】本题主要考查了金属材料的选择依据和书写化学方程式、文字表达式、电离方程式的相关知识点,需要掌握黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属;注意:a、配平 b、条件 c、箭号才能正确解答此题.

 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案