题目内容
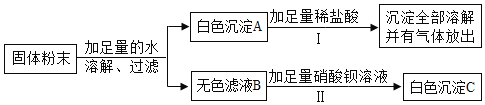
【题目】化学兴趣小组的同学在实验室中用加热4.9g氯酸钾和1.58g高锰酸钾混合物的方法进行了制取氧气的研究,得到如图所示的曲线图。试回答:
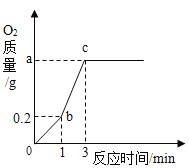
(1)b点得到的氧气主要是由分解_____(填氯酸钾或高锰酸钾)产生的,b-c段产生氧气的速度明显比0-b段加快,其原因是_____。
(2)c点对应产生氧气的质量a值是_____g。
(3)反应结束后所得固体混合物中质量分数最大的物质的质量分数是多少?_____
【答案】高锰酸钾 高锰酸钾分解产生的二氧化锰作为催化剂,加速了氯酸钾的分解 2.08 固体混合物中KCl的质量分数最大,其数值为67.73%
【解析】
根据题目图像及氯酸钾和高锰酸钾制氧气的反应综合进行分析解答。
(1)氯酸钾和高锰酸钾混合加热时,高锰酸钾会先受热分解为锰酸钾、二氧化锰和氧气,故b点得到的氧气主要是由分解高锰酸钾产生的,然后氯酸钾在二氧化锰作催化剂的的条件下快速分解,故b-c段产生氧气的速度明显比0-b段加快,其原因是高锰酸钾分解产生的二氧化锰作为催化剂,加速了氯酸钾的分解。
(2)解:设氯酸钾反应生成的氧气质量为x,高锰酸钾反应生成的氧气质量为y。
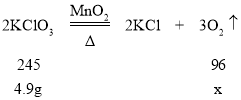 ,
,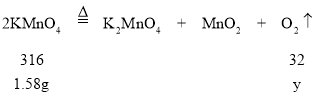
故:![]() ,x=1.92g;
,x=1.92g;![]() ,y=0.16g;
,y=0.16g;
c点表示为高锰酸钾和氯酸钾反应生成的氧气的总质量,故a=1.92+0.16=2.08。
(3)由题(2)及质量守恒定律可知氯酸钾反应生成的氯化钾质量为4.9g-1.92g=2.98g,其质量大于了高锰酸钾的质量,故生成物中质量最大的为氯化钾,剩余物总质量为4.9g+1.58g-2.08g=4.4g, 则氯化钾的质量分数为![]()

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目